
| A. | HCN | B. | CH3COOH | C. | HNO2 | D. | HF |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:实验题
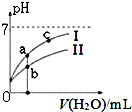 “8.12”天津港爆炸中有一定量的氰化物泄露.氰化物多数易溶于水,有剧毒,易造成水污染.为了增加对氰化物的了解,同学们查找资料进行学习和探究.
“8.12”天津港爆炸中有一定量的氰化物泄露.氰化物多数易溶于水,有剧毒,易造成水污染.为了增加对氰化物的了解,同学们查找资料进行学习和探究.| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数( 25℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 他们的组成元素是相同的 | |
| B. | 耐腐蚀的性能不同 | |
| C. | 它们都属于钢,因此物理性质相同 | |
| D. | 构成普通钢和不锈钢的主要元素都是铁,因此它们的化学性质相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
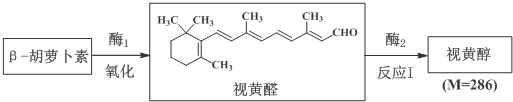
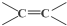 $\stackrel{氧化}{→}$
$\stackrel{氧化}{→}$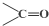 +
+
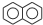 ,C10H8)的衍生物,其可能具有的化学性质有bd(选填编号).
,C10H8)的衍生物,其可能具有的化学性质有bd(选填编号).
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇的官能团是:-OH | B. | 乙醇的分子式是:CH3CH2OH | ||
| C. | 乙烯的结构简式是:CH2CH2 | D. | 乙烯无官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
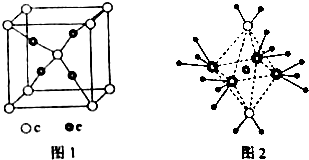
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 1 | 2 | 3 | 4 | 5 | 6 | … |
| C2H4 | C2H6 | C2H6O | C3H6 | C3H8 | C3H8O | … |
| A. | C6H14 | B. | C7H14 | C. | C7H16 | D. | C7H16O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com