
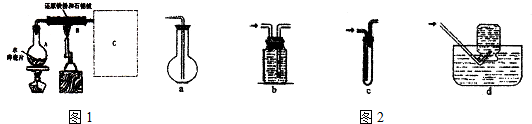
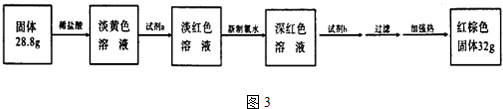
���� I����1��װ��B�У�ˮ���������۸����·���������ԭ��Ӧ������Fe3O4��������
��2�������ܶȱȿ���С�������ſ������ռ���Ӧ�������ſշ���Ҳ������ˮ���ռ���
II���õ���������Ϊ28.8g���������ϡ�����ַ�Ӧ���õ�dz��ɫ��Һ��ӦΪFeCl3�������Լ�a��Ϊ����ɫ���������Լ�ΪKSCN���������Ʊ���ˮ����Һ��ɫ���˵��Fe3+Ũ������Fe2+����ˮ��������Fe3+��Ȼ���������������Һ���ɵõ������������壬�����ˡ���ǿ�ȣ��ɷֽ����ɺ���ɫ���������壻
��ȡ������ɫ�����Һ���ٵμӹ���KSCN��Һ��������ֺ�ɫ��˵����KSCN��������֮+3������������
��4������ɫ����Ϊ���������ɸ����������㣮
��� �⣺I��װ��B�У�ˮ���������۸����·���������ԭ��Ӧ������Fe3O4������������ʽΪ3Fe+4H2O��g�� $\frac{\underline{\;\;��\;\;}}{\;}$Fe3O4+4H2��������������ˮ��������ˮ���ռ���bdΪ��ˮ�����������ܶȱȿ���С��a��c���������ռ�������
�ʴ�Ϊ��3Fe+4H2O$\frac{\underline{\;\;��\;\;}}{\;}$Fe3O4+4H2���� bd��
��1���õ���������Ϊ28.8g���������ϡ�����ַ�Ӧ���õ�dz��ɫ��Һ��ӦΪFeCl3�������Լ�a��Ϊ����ɫ���������Լ�ΪKSCN���������Ʊ���ˮ����Һ��ɫ���˵��Fe3+Ũ������Fe2+����ˮ��������Fe3+��Ȼ���������������Һ���ɵõ������������壬�����ˡ���ǿ�ȣ��ɷֽ����ɺ���ɫ���������壬
�ʴ�Ϊ��KSCN��NaOH��
��2������������ˮ����Һ��ɫ�����ԭ�����������ӱ�����������ʽΪ2Fe2++Cl2=2Fe3++2Cl-���ʴ�Ϊ��2Fe2++Cl2=2Fe3++2Cl-��
��3����ijͬѧ��ʵ���м����˹�����ˮ������һ��ʱ��������ɫ��ȥ������ԭ����+3������������SCN-����������ˮ������
�ʴ�Ϊ��SCN-����������ˮ������
��Ϊ�˶�������ļ���2������֤��ʵ�鷽���ǿ�ȡ������ɫ�����Һ���ٵμӹ���KSCN��Һ��������ֺ�ɫ��˵����KSCN��������֮+3������������
�ʴ�Ϊ��ȡ������ɫ�����Һ���μӹ���KSCN ��Һ��������ֺ�ɫ����˵������2 ��ȷ��������죬�����2 ����ȷ��
��4������ɫ����Ϊ������������Ϊ32g����m��Fe��=$\frac{56��2}{56��2+16��3}$��32g=22.4g���أ�Fe��=$\frac{22.4}{28.8}$=77.8%���ʴ�Ϊ��77.8%��
���� ���⿼�����ʵĺ����ⶨ�Լ�����ʵ�鷽������ƣ�Ϊ�߿��������ͣ���Ŀ�����Լ��仯������ת��Ϊ���壬������ʵ�鷽����������ۣ���Ŀ�Ѷ��еȣ�ע�����ʵ��ԭ����ʵ��Ŀ�ģ�


 �Ǽ�����������ϵ�д�
�Ǽ�����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ԭ��صĸ����͵��ص������϶�����ʧ���ӵ�������Ӧ | |
| B�� | �ö��Ե缫���Na2SO4��Һ������������������ʵ���֮��Ϊ1��2 | |
| C�� | �ö��Ե缫��ⱥ��NaCl��Һ������0.1 mol����ת�ƣ�������0.1 mol NaOH | |
| D�� | �Ʋ������п����ȶ����������ʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
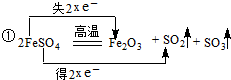 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
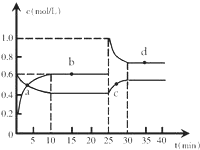 �ں��º��������£���һ����NO2��N2O4�Ļ������ͨ���ݻ�Ϊ2L���ܱ������з�����Ӧ��N2O4 ��g��?2NO2 ��g����H��0����Ӧ�����и����ʵ����ʵ���Ũ��c��ʱ��t�ı仯��ϵ��ͼ��ʾ��
�ں��º��������£���һ����NO2��N2O4�Ļ������ͨ���ݻ�Ϊ2L���ܱ������з�����Ӧ��N2O4 ��g��?2NO2 ��g����H��0����Ӧ�����и����ʵ����ʵ���Ũ��c��ʱ��t�ı仯��ϵ��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | ʵ������ | ʵ������ | ���ӷ���ʽ | ʵ����� |
| �� | ��FeCl2��Һ�е���������ˮ | ��Һ��dz��ɫ��Ϊ��ɫ | 2Fe2++Cl2=2Fe3++2Cl- | Fe2+���л�ԭ�� |
| �� | ��FeCl3��Һ�м����������� | ��Һ�ɻ�ɫ��Ϊdz��ɫ | Fe+2Fe3+=3Fe2+ | Fe3+���������� |
| �� | ��FeCl3��Һ�е�������KI��Һ�͵�����Һ | ��Һ���ձ�Ϊ��ɫ | 2Fe3++2I-�T2Fe2++I2 | Fe3+���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
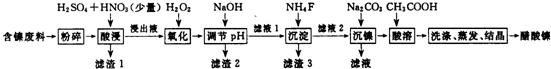
| ��1 | ��2 | |||
| ���� | ��ʼ������pH | ������ȫ��pH | ���� | 20��ʱ�ܽ��ԣ�H2O�� |
| Fe3+ | 1.1 | 3.2 | CaSO4 | �� |
| Fe2+ | 5.8 | ����8.8 | NiF | ���� |
| Al3+ | 3.0 | 5.0 | CaF2 | ���� |
| Ni2+ | 6.7 | 9.5 | NiCO3 | KSP=9.60��10-6 |
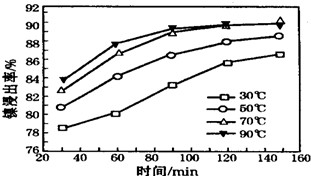
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ���� | �״� | ������ | ��������� |
| �е�/�� | 65 | 249 | 199.6 |
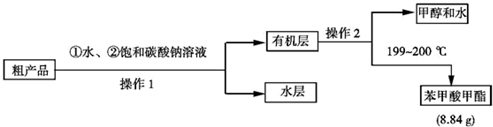
| ������Ŀ | ʵ�������� |
| ����ֲ�Ʒ�к���ˮ�IJ����� | |
| ����ֲ�Ʒ�к�������IJ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu2+ Cl- K+ SO42- | B�� | Na+ NO3 - OH - CO3 2- | ||
| C�� | Ba2+ Cl- NO3 - SO4 2- | D�� | K+ Na+ Cl- SO4 2- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com