
分析 (1)双氧水能被高锰酸钾氧化为氧气单质;
(2)反应中没有元素化合价的变化;
(3)化合价升高元素失去电子,被氧化,所在反应物是还原剂,对应产物是氧化产物;化合价降低元素得到电子,被还原,所在的反应物是氧化剂,对应产物是还原产物;
(4)根据方程式中物质的物质的量关系计算.
解答 解:(1)化合价降低元素所在的反应物是氧化剂,KMnO4中Mn化合降低,所以是氧化剂,双氧水能被高锰酸钾氧化为氧气单质,
故答案为:O2;
(2)SbCl5+HF═SbF5+5HCl反应中没有元素化合价的变化,不是氧化还原反应,
故答案为:否;
(3)反应2K2MnF6+4SbF5→4KSbF6+2MnF3+F2↑中,K2MnF6中Mn元素的化合价降低,所以K2MnF6是氧化剂,SbF5中F元素化合价升高,被氧化,所以SbF5是还原剂,故答案为:K2MnF6;F;
(4)2K2MnF6+4SbF5═4KSbF6+2MnF3+F2↑,反应中生成1molF2时,消耗2molKMnO4;
故答案为:2mol.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:解答题
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
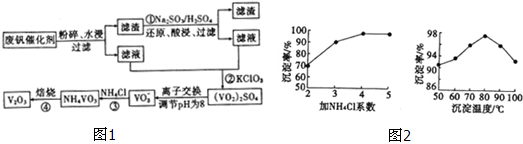
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
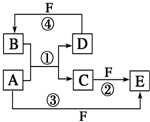 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
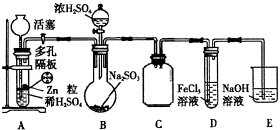
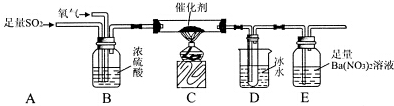
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 | |
| B. | HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 | |
| C. | Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 | |
| D. | 分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C4H10和C20H42 | B. | 邻二甲苯和对二甲苯 | ||
| C. | C4H8和C3H6 | D. | C2H2和C4H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
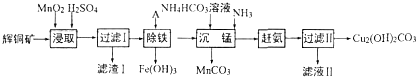
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com