
| A、从1 L 1 mol/L的NaCl溶液中取出100 mL,其浓度为0.1 mol/L |
| B、配制0.5 L 10 mol/L的盐酸,需要氯化氢气体112 L |
| C、0.5 L 2 mol/L BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 |
| D、10 g 98%的硫酸(密度为1.84 g/cm3)与10 mL 18.4 mol/L硫酸的浓度是不同的 |
| N |
| NA |
| 1000ρω |
| M |
| 1000×1.84g/L×98% |
| 98g/mol |


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
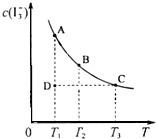 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq) 某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq) 某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )| A、反应I2(aq)+I-(aq)?I3-(aq)的△H>0 |
| B、若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1<K2 |
| C、若反应进行到状态D时,平衡向逆反应方向移动 |
| D、状态B与状态C相比,状态C的c(I2)大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.37 mol |
| B、0.63mol |
| C、0.75mol |
| D、1.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
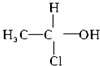 .下列化合物中存在对映异构体的是( )
.下列化合物中存在对映异构体的是( )| A、C2H5CH=CHCH(CH3)-CH=CHC2H5 |
B、  |
| C、甲酸 |
| D、C6H5CH(CH3)OCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol/L硫酸溶液所含的H+数约为1.204×1024个 |
| B、标准状况下气体摩尔体积约为22.4L |
| C、0.5 L 1 mol/L FeCl3溶液与0.2 L 1 mol/L KCl溶液中的Cl-的数目之比为15:2 |
| D、100 mL 1 mol/L NaCl溶液与50 mL 1 mol/L AlCl3溶液中Cl-物质的量浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg2+、Ca2+、HCO3-、Cl- |
| B、Na+、Mg2+、Cl-、SO42- |
| C、K+、Fe3+、Cl-、SO42- |
| D、Ba2+、Al3+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
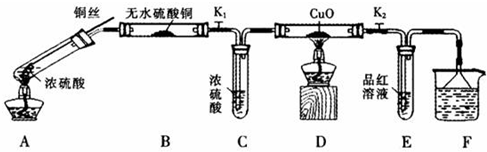
| 硫酸/mol?L-1 | 黑色物质出现的温度/℃ | 黑色物质消失的温度/℃ |
| 15 | 约150 | 约236 |
| 16 | 约150 | 约250 |
| 18 | 约120 | 不消失 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com