
分析 (1)根据n=$\frac{V}{{V}_{m}}$=$\frac{m}{M}$=$\frac{N}{NA}$结合物质的构成计算相关物理量;
(2)${\;}_{1}^{1}$H和${\;}_{8}^{18}$O构成的水摩尔质量为(1×2+18)g/mol,然后根据n=$\frac{m}{M}$,一个水分子中含有10个中子;
(3)根据n=cV和m=nM来计算,根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析.
解答 解:(1)m(O2)=0.3mol×32g/mol=9.6g,m(O3)=0.2mol×48g/mol=9.6g,它们的质量之比为1:1;
由n=$\frac{N}{NA}$可知结合它们所含的原子数之比为0.3mol×2:0.2mol×3=1:1;
由n=n=$\frac{V}{{V}_{m}}$可知,它们的体积之比为0.3:0.2=3:2;
由ρ=$\frac{M}{Vm}$可知,它们的密度之比等于相对分子质量之比,为32:48=2:3,
故答案为:1:1;1:1;3:2;2:3;
(2)由${\;}_{1}^{1}$H和${\;}_{8}^{18}$O构成的水摩尔质量为(1×2+18)g/mol,n=$\frac{m}{M}$=$\frac{10g}{20g/mol}$=0.5mol,中子的物质的量为0.5mol×10=5mol,
故答案为:20g/mol;0.5mol;5;
(3)配制0.1mol•L-1 NaOH溶液480ml,由于无480mL容量瓶,故应选用500mL容量瓶,所需的氢氧化钠的物质的量n=cV=0.1mol/L×0.5L=0.05mol,质量m=nM=0.05mol×40g/mol=2.0g;定容时俯视刻度线,会导致溶液体积偏小,则浓度偏大,若NaOH溶液在转移至容量瓶时,洒落了少许,溶质损失,浓度偏小,
故答案为:2.0;大于;小于.
点评 本题考查物质的量的相关计算,误差分析,侧重于学生的分析能力和计算能力的考查,注意把握相关计算公式的运用,难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
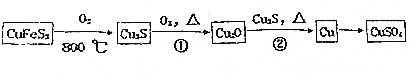
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 当该卤代烃发生取代反应时,被破坏的键是①和③ | |
| B. | 当该卤代烃发生消去反应时,被破坏的键是①和③ | |
| C. | 当该卤代烃发生水解反应时,被破坏的键② | |
| D. | 当该卤代发生消去反应时,被破坏的键是①和② |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| 温度 实验次数 | 起始温度t1/℃ | 终止温度t℃/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | 4.0 |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为两套实验装置.
如图为两套实验装置.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
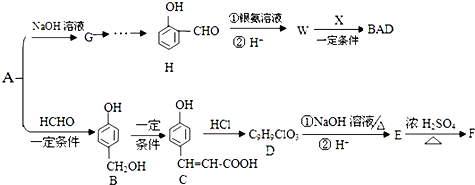
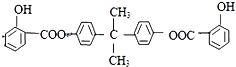
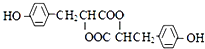
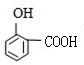 .
.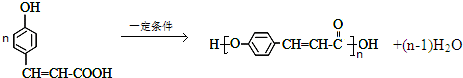 .
. .
.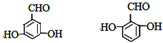 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素原子中共有25个电子 | B. | 该元素原子核外有4个能层 | ||
| C. | 该元素原子最外层共有2个电子 | D. | 该元素原子M电子层共有8个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com