
【题目】我们利用物质的结构与性质对周期表进行研究,有助于我们更好地掌握同类知识。
(1)基态砷原子中,价电子占用_________个原子轨道;雌黄分子式为As2S3,分子结构如图,则As原子的杂化方式为_________ 。

(2)N2与CO互为等电子体,则1molCO分子中含有的π键数目是_________个。
(3)向CuSO4溶液中加人少量氨水生成蓝色沉淀,继续加人过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加人一定量乙醇,析出[Cu(NH3)4]SO4 .H2O晶体;该晶体所含的非金厲元素中,N、O、S第一电离能由大到小的顺序是_________ (填元素符号),SO42-的空间构型为____________,晶体中含有的化学键有__________。加人乙醇后析出[Cu(NH3)4]SO4 .H2O晶体的原因是____________。
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如下左图所示,由A、B两种微粒构成。 将其加热至148℃熔化,形成一种能导电的熔体。已知A微粒与CCl4具有相同的空间构型和相似的化学键特征,则A为_________ , B为_______________。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,下右图为其立方晶胞。已知晶体中最近的硼原子和磷原子核间距为x cm,磷化硼的摩尔质量为bg.·mol-1,阿伏加德罗常数为NA,则磷化硼晶体密度的表达式
为____________g.cm-3。(列出计算式即可)

【答案】 4 sp3杂化 2NA(或2×6.02×1023) N>O>S 正四面体 离子键、极性共价键和配位键 乙醇分子极性比水分子极性弱,加入乙醇降低溶剂的极性,从而减小溶质的溶解度 PCl4+ PCl6- ![]()
【解析】(1)基态砷原子中,价电子排布式为4s24p3,根据洪特规则,4p轨道的3个电子要分占不同的轨道并且自旋状态相同,所以其价电子共占用4个原子轨道;由雌黄分子结构示意图可知,每个As原子与3个S原子形成3个σ键,由于其价电子数是5个,所以该分子中砷原子有1个孤电子对,根据价层电子对互斥理论,中心原子的价电子对数为4,所以中心原子的杂化方式为sp3杂化。
(2)N2与CO互为等电子体,氮气分子中有叁键,叁键中有1个σ键、2个π键,等电子体之间结构相似,所以CO分子中也有2个π键,则1molCO分子中含有的π键数目是2NA(或2×6.02×1023)个。
(3) 一般非金属性越强的元素的第一电离能也越大,但是每个周期的IIA(s轨道全满)和VA(p轨道半充满)元素因其原子结构的特殊性,其第一电离能高于相邻元素,所以N、O、S第一电离能由大到小的顺序是N>O>S。SO42-的中心原子价电子对数n=![]() =4,中心原子形成了4个σ键,所以其空间构型为正四面体。[Cu(NH3)4]SO4H2O晶体是一种配合物,其内界中中心原子铜离子和配体氨分子之间形成配位键,氨分子内有极性键,外界硫酸根与内界之间形成离子键。加人乙醇后析出[Cu(NH3)4]SO4H2O晶体的原因是乙醇分子极性比水分子极性弱,加入乙醇降低溶剂的极性,从而减小溶质的溶解度。
=4,中心原子形成了4个σ键,所以其空间构型为正四面体。[Cu(NH3)4]SO4H2O晶体是一种配合物,其内界中中心原子铜离子和配体氨分子之间形成配位键,氨分子内有极性键,外界硫酸根与内界之间形成离子键。加人乙醇后析出[Cu(NH3)4]SO4H2O晶体的原因是乙醇分子极性比水分子极性弱,加入乙醇降低溶剂的极性,从而减小溶质的溶解度。
(4) A微粒与CCl4具有相同的空间构型和相似的化学键特征,所以A与四氯化碳是等电子体,则A为PCl4+ ,由质量守恒和电荷守恒可知 B为PCl6- 。
(5)该晶胞中含有4个B原子和4个P原子。如果把晶胞分成8个相同的小立方,则B原子恰好可以位于其中4个小立方的体心,设晶胞的边长为2a,晶体中最近的硼原子和磷原子核间距为x cm,则xcm= ![]() ,所以a=
,所以a= ![]() ,1mol该晶胞的体积为
,1mol该晶胞的体积为![]() =
=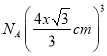 ,磷化硼的摩尔质量为bg.·mol-1,则1mol该晶胞中含BP 4mol,其质量为4bg,所以磷化硼晶体密度的表达式 为
,磷化硼的摩尔质量为bg.·mol-1,则1mol该晶胞中含BP 4mol,其质量为4bg,所以磷化硼晶体密度的表达式 为![]() g.cm-3。
g.cm-3。


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】钛矿工业中会排放出酸性废水。含石TiO2+、Fe2+、Fe3+离子,其综合利用如下:

已知:TiO2+易水解,只能存在于强酸性溶液中。
(1)写出步骤Ⅰ发生反应的离子方程式___________。
(2)步骤Ⅰ后所得溶液中Fe2+的检验方法是___________。
(3)从溶液中得到FeSO4·7H2O的操作是___________、___________、过滤、洗涤。步骤Ⅲ中反应温度一般需控制在35℃以下,其目的是___________。
(4)步骤Ⅳ发生反应的化学方程式为___________。
(5)步骤Ⅲ中,FeCO3达到溶解平衡时,若室温下测得溶液的pH为8.5,c(Fe2+)=1×10-6mol·L-1。试判断所得的FeCO3中___________(填“有”或“没有”)(己知Fe(OH)2(已知Fe(OH)2的Ksp为8×10-16)
(6)向“富TiO2+溶液”中加入Na2CO3粉末得到固体TiO2·nH2O。请用化学原理解释其原因。___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推论正确的是
A. NH![]() 为正四面体结构,可推测PH
为正四面体结构,可推测PH![]() 也为正四面体结构
也为正四面体结构
B. SiH4的沸点高于CH4,可推测PH3的沸点高于NH3
C. CO2为非极性分子,可推测SO2也为非极性分子
D. C2H6是碳链为直线型的非极性分子,可推测C3H8也是碳链为直线型的非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某容积为2L的密闭容器内,某一反应中M(g)、N(g)的物质的量随反应时间变化的曲线如图,依图所示:
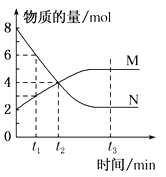
(1)该图形所描述的反应的化学方程式是______________。
(2)在图上所示的三个时刻中,_______(填t1、t2或t3)时刻处于平衡状态,此时v正____v逆(填>、<或=)。
(3)下列描述中能说明上述反应达到平衡状态的是_______。
A.容器中M与N的物质的量之比为1:l
B.混合气体的密度不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内消耗2molN的同时生成ImolM
(4)下列措施能增大反应速率的是_______(选填字母)
A.升高温度 B.降低压强 C.减小M的浓度 D.将反应容器体积缩小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________________。
(2)根据元素周期律,原子半径Ga_____________As,第一电离能Ga____________As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________________,其中As的杂化轨道类型为_________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_____________________。
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________,Ga与As以________键键合。Ga和As的摩尔质量分别为MGa g·mol-1和MAs g·mol-1,原子半径分别为rGa pm和rAs pm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标况下,将一装满NO2气体的试管倒置在水槽中,可见试管中液面逐渐上升,反应结束后,试管中所得溶液的物质的量浓度为(忽略溶质的扩散)( )
A. 1 mol/L B. 22.4 mol/L C. 0.045 mol/L D. 0.03 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钙是一种阻锈剂,可用于染料工业,某兴趣小组拟制备Ca(NO2)2并对其性质进行探究。
【背景素材】
I.NO+NO2+Ca(OH)2=Ca(NO2)2+H2O。
Ⅱ.Ca(NO2)2能被酸性KMnO4溶液氧化成NO3-,MnO4-被还原为Mn2+。
Ⅲ.在酸性条件下,Ca(NO2)2能将I-氧化为I2,S2O32-能将I2还原为I-。
【制备氮氧化物】
(1)甲组同学拟利用如下左图所示装置制备氮氧化物。

①仪器X、Y的名称分别是______________、______________。
②装置B中逸出的NO与NO2的物质的量之比为1∶1,则装置B中发生反应的化学方程式为_____________________ ,若其他条件不变,增大硝酸的浓度,则会使逸出的气体中n(NO2)__________n(NO)(填“>”或“<”)。
【制备Ca(NO2)2】
⑵乙组同学拟利用装置B中产生的氮氧化物制备Ca(NO2)2,装置如上右图。
①装置C中导管末端接一玻璃球的作用是________________。
②装置D的作用是______________;装置E的作用是________________。
【测定Ca(NO2)2的纯度】
⑶丙组同学拟测定Ca(NO2)2的纯度(杂质不参加反应),可供选择的试剂:
a.稀硫酸 b. c1mol·L-1的KI溶液 c.淀粉溶液
d.c2mol·L-1的Na2S2O3溶液 e.c3mol·L-1 的酸性 KMnO4 溶液
①利用Ca(NO2)2的还原性来测定其纯度,可选择的试剂是______________(填字母)。
②利用Ca(NO2)2的氧化性来测定其纯度的步骤:准确称取mgCa(NO2)2样品放入锥形瓶中,加适量水溶解,__________________(请补充完整实验步骤)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式或电离方程式的书写正确的是()
A. NaHSO4熔融:NaHSO4=Na++HSO4-
B. Al(OH)3酸式电离: Al(OH)3= H++AlO2- + H2O
C. 向Na2S溶液中滴入少量稀盐酸:S 2-+2H+=H2S↑
D. Ca(HCO3)2溶液与过量NaOH溶液反应:OH-+HCO![]() +Ca2+=CaCO3↓+H2O
+Ca2+=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
氯贝特(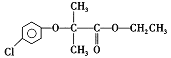 )是临床上一种抗血栓药物,它的一种合成路线如图28(图中部分反应条件及部分反应物、生成物已略去)。
)是临床上一种抗血栓药物,它的一种合成路线如图28(图中部分反应条件及部分反应物、生成物已略去)。
回答下列问题: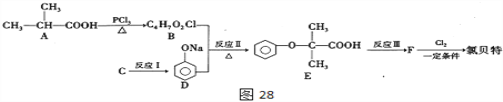
(1)有机物A命名为________,反应II的反应类型为_________,E分子中含有的官能团名称是___________。
(2)要实现反应I的转化,加入下列物质能达到目的有__________。
a. NaHCO3 b. NaOH c.Na2CO3 d. CH3COONa
(3)写出反应Ⅲ的化学方程式__________________________________ 。
(4)产物E有多种同分异构体,满足下列条件的所有同分异构体G有______种。
① 属于酯类且与FeCl3溶液显紫色 ② 能发生银镜反应
③ 1molG最多与2molNaOH反应 ④ 苯环上只有2个取代基且处于对位
其中核磁共振氢谱有五组峰的有机物结构简式为______________________。
(5)结合以上合成路线信息,设计以CH3CH2COOH为原料(无机试剂任选),合成有机物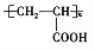 的合成流程。____________
的合成流程。____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com