
下列离子方程式正确的是
A.将一定量KAl(SO4)2溶液和一定量Ba(OH)2溶液混合,沉淀的质量恰好最大时:Al3++2SO42-+3OH-+2Ba2+=2BaSO4↓+Al(OH)3↓
B.KMnO4与浓盐酸反应制Cl2:2MnO4-+16HCl=2Mn2++6Cl-+5Cl2↑+8H2O
C.0.1molCl2和100mL1mol/LFeBr2反应:3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2
D.用Al(OH)3中和过多的胃酸:Al(OH)3+3H+=Al3++3H2O
科目:高中化学 来源:2016届辽宁省高三上学期12月模拟化学试卷(解析版) 题型:选择题
下列反应的离子方程式不正确的是
A.向NaClO溶液中通入少量SO2气体:3ClO-+SO2+H2O═SO42-+Cl-+2HCl
B.将过量的Cl2通入FeBr2溶液中:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2
C.向碳酸氢钙溶液中滴加氢氧化钠溶液至Ca2+恰好完全:Ca2++HCO3-+OH-=CaCO3↓+H2O
D.向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液至沉淀量最大:
NH4++Al3++2SO42-+4OH-=Al(OH)3↓+2BaSO4↓+NH3·H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北邯郸魏县一中、曲周县一中高一上期中化学试卷(解析版) 题型:选择题
下列物质按照单质、化合物、混合物顺序排列,其中物质类型排列顺序正确的是
A.氯水、氯化钾、胆矾
B.液溴、水和冰混合、澄清石灰水
C.氮气、净化后的空气、氧化镁
D.白磷、生锈的铁钉、高锰酸钾充分加热后的剩余固体
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北邯郸魏县一中、曲周县一中高二上期中化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.常温下,反应C(s) + CO2(g)=2CO(g)不能自发进行,则该反应△H>0
B.强电解溶液的导电能力一定强于弱电解质溶液的导电能力
C.CH3COOH、Cu(OH)2、BaSO4、NH3都是常见的弱电解质
D.常温下就能发生的化学反应一定是放热反应
查看答案和解析>>
科目:高中化学 来源:2016届四川省宜宾市高三上学期第10周周练化学试卷(解析版) 题型:填空题
Ⅰ.CO和H2作为重要的燃料和化工原料,有着十分广泛的应用。
(1)已知:C(s)+O2(g)=CO2(g) △H1= -393.5 kJ·mol-1
C(s)+H2O(g)= CO(g)+H2(g) △H2= +131.3 kJ·mol-1
则反应CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g)△H= kJ·mol-1。
(2)利用反应CO(g)  +H2(g)+O2(g) = CO2(g) +H2O(g) 设计而成的MCFS燃料电池是用水煤气(CO和H2物质的量之比为1:1)作负极燃气,空气与CO2的混合气为正极助燃气,用一定比例的Li2CO3和Na2CO3低熔点混合物做电解质的一种新型电池。现以该燃料电池为电源,以石墨作电极电解饱和NaCl溶液,反应装置以及现象如图所示。则有:
+H2(g)+O2(g) = CO2(g) +H2O(g) 设计而成的MCFS燃料电池是用水煤气(CO和H2物质的量之比为1:1)作负极燃气,空气与CO2的混合气为正极助燃气,用一定比例的Li2CO3和Na2CO3低熔点混合物做电解质的一种新型电池。现以该燃料电池为电源,以石墨作电极电解饱和NaCl溶液,反应装置以及现象如图所示。则有:
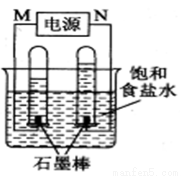
①燃料电池即电源的N极的电极反应式为 _______________________;
②已知饱和食盐水的体积为1 L,一段时间后,测得左侧试管中气体体积为11.2 mL(标准状况),若电解前后溶液的体积变化忽略不计,而且电解后将溶液混合均匀,则此时溶液的pH为  。
。
Ⅱ.CO和NO是汽车尾气的主要污染物。消除汽车尾气的反应式之一为:
2NO(g)+2CO (g)
(g)  N2(g)+2CO2(g)。请回答下列问题:
N2(g)+2CO2(g)。请回答下列问题:
(3)一定温度下,在一体积为VL的密闭容器中充人一定量的NO和CO时,反应进行到t时刻时达到平衡状态,此时n(CO)=amol、n(N0)=2amol、n(N2)=bmol,且N2占平衡混合气体总体积的1/4。
①该反应的平衡常数K= (用只含a、V的式子表示)
②判断该反应达到平衡的标志是____(填序号)
A.v(CO2)生成=v(CO)消耗
B.混合气体的平均相对分子质量不再改变
C.混合气体的密度不再改变
D.NO、CO、N2、CO2的物质的量浓度均不再变化
(4)在一定温度下,将2.0molNO、2.4molCO通入固定容积2L的密闭中,反应过程中部分物质的物质的量变化如图所示,则:
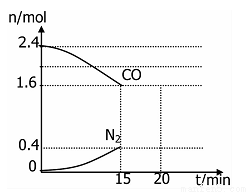
①有害气体NO的转化率是 ,0~15minCO2的平均反应速率v(CO2)=____(保留小数点后三位)。
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件是 。(填序号)。
A.增加CO的量 B.加入催化剂 C.减小容器体积 D.扩大容器体积
查看答案和解析>>
科目:高中化学 来源:2016届北京一五六中学上学期高三期中考试化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数,下列说法正确的是
A.1 mol OH- 中含有10NA个电子
B. 46g的NO2气体中含有NA个NO2分子
C.1 L 1 mol/L的AlCl3溶液中含有NA个Al3+
D.常温常压下11.2 L的甲烷气体含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省盐城市高一上学期期中考试化学试卷(解析版) 题型:选择题
在通常情况下,稀有气体很难与其他元素发生化学反应,其原因是
A.稀有气体最外层电子数均为8个,很稳定
B.稀有气体的电子层数比较多,很稳定
C.稀有气体的最外层电子数均达到稳定结构
D.稀有气体的原子核所带电荷较多
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上第二次月考化学试卷(解析版) 题型:填空题
现有下列物质:
①干冰 ②NaHCO3晶体 ③氨水 ④纯醋酸
⑤FeCl3溶液 ⑥铜 ⑦ Fe(OH)3胶体 ⑧蔗糖,
(1)其中属于电解质的是 ,
(2)写出FeCl3的电离方程式:__________________________,
(3)写出NaHCO3(aq) 与稀盐酸反应的离子方程式:_____________________,
(4)胶体是一种常见的分散系,回答下列问题。
①向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,
停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体化学反应方程式为 。
②向Fe(OH)3胶体中加入Na2SO4饱和溶液,由于_______离子(填离子符号)的作用,使胶体形成了沉淀,这个过程叫做胶体的聚沉。
③区分胶体和溶液常用的方法叫做 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com