

���� �����Ȼ�����ˮ��������ˮ���ڸ����·�Ӧ����������������������Ϊ��ֹ����Ӧ�ķ�����������Ҫ�����β�����봦����ֹ��Ⱦ�������������Ȼ��������������ռ�ʱ�轵��ʹ֮��ȴ�ᾧ������ͬʱ�����ø��������Ȼ�����Һ��������������������Ȼ���������ȥ�������壬�ݴ˷������⣻
��1��Ҫʹ������FeCl3�����ռ���������FeCl3���������������ʣ�
��2����ֹFeCl3���⣬����ˮ�����Ӵ���
��3��B�е���ˮ����Ϊ����ȴFeCl3ʹ������������ռ���Ʒ��
��4�����������������ԣ�������л�ԭ�ԣ�����֮�䷢��������ԭ��Ӧ��
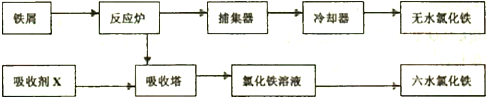
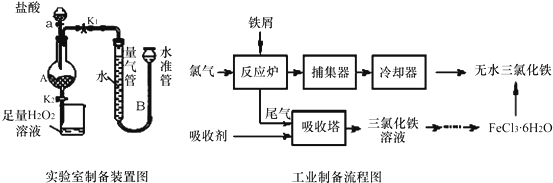
��5�����������ڷ�Ӧ¯�з�Ӧ�����Ȼ�����β�������ռ�Q�����õ��Ȼ�������QΪ�Ȼ��������Ȼ�����Һ����Ũ������ȴ�ᾧ�õ��Ȼ������壬Ϊ��ֹ�Ȼ���ˮ�⣬��HCl�����м��������Ȼ�������õ��Ȼ�����
��β���к����������ɹ������̿�֪������ˮ��X�������������������������Ȼ�����������ˮ��XΪ�Ȼ�������
�۵�������������ݴ�ѡ��ָʾ����VmLNa2S2O3��Һ����Na2S2O3���ʵ���ΪV•10-3 L��cmol/L=c•V•10-3 mol��mg��Ʒ��Ҫ0.01cVmolNa2S2O3�����ݹ�ϵʽ2Fe3+��I2��S2O32-����n��Fe3+�����Ȼ��������ʵ�������n��Fe3+��������m=nM�����Ȼ�����������������������������㣻
��� �⣺��1����FeCl3���ȷ�������ʹ������FeCl3�����ռ������ʴ�Ϊ���ڳ�����FeCl3�����·����ȣ�
��2��Ϊ��ֹFeCl3��������ȡ�Ĵ�ʩ�Т�ͨ������Cl2���ø����N2�Ͼ�Cl2����ѡ���ڢݣ�
��3��B�е���ˮ����Ϊ����ȴFeCl3ʹ������������ռ���Ʒ���ʴ�Ϊ����ȴ��ʹFeCl3�����������ռ���Ʒ��
��4�����������������ԣ�������л�ԭ�ԣ�����֮�䷢��������ԭ��Ӧ��2FeCl3+H2S=2FeCl2+2HCl+S�������ӷ���ʽΪ��2Fe3++H2S=2Fe2++S��+2H+��
�ʴ�Ϊ��2Fe3++H2S=2Fe2++S��+2H+��
��5�����������ڷ�Ӧ¯�з�Ӧ�����Ȼ�����β�������ռ�Q�����õ��Ȼ�������QΪ�Ȼ��������Ȼ�����Һ����Ũ������ȴ�ᾧ�õ��Ȼ������壬Ϊ��ֹ�Ȼ���ˮ�⣬��HCl�����м��������Ȼ�������õ��Ȼ�����
���������з�����Ӧ�����ӷ���ʽΪ��2Fe2++Cl2=2Fe3++2Cl-���ʴ�Ϊ��2Fe2++Cl2=2Fe3++2Cl-��
�۵�����������������ѡ�������Ϊָʾ����VmLNa2S2O3��Һ����Na2S2O3���ʵ���ΪV•10-3 L��cmol/L=c•V•10-3 mol����
���ݹ�ϵʽ��2Fe3+��I2��2S2O32-
2 2
n��Fe3+�� c•V•10-3mol��10
���� n��Fe3+��=c•V•10-3 mol��10=0.01cVmol��
����m����ˮ�Ȼ�����Ʒ���Ȼ���������Ϊ0.01cVmol��162.5g/mol=1.625cVg
����m����ˮ�Ȼ�����Ʒ���Ȼ�������������Ϊ$\frac{1.625cVg}{mg}$��100%=$\frac{162.5cV}{m}$%��
�ʴ�Ϊ��������Һ��$\frac{162.5cV}{m}$%��
���� ���⿼��ѧ���Թ������̵����⣬�漰���ʵķ����ᴿ�������ˮ�⼰�ζ�ԭ����Ӧ������㣬�Ѷ��еȣ���Ҫѧ��������ʵ�Ļ���֪ʶ���������֪ʶ��������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��һ��Ԫ����ɵ�����һ���ǵ��� | |
| B�� | �����ܵ����H+�Ļ����ﶼ���� | |
| C�� | ���ܵ����OH-��ʹ��Һ�Լ��ԣ�����Һ�Լ��ԵIJ�һ���Ǽ� | |
| D�� | ������ˮ�γɵ���Һ�ܵ��磬�����ǵ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
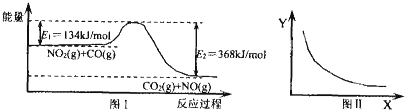
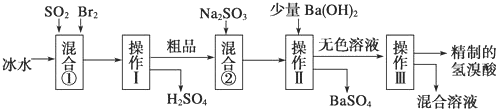
| A�� | �÷�Ӧ���ʱ��H=+234 kJ•mol-1 | |
| B�� | ��X��ʾ�¶ȣ���Y��ʾ�Ŀ�����CO2�����ʵ���Ũ�� | |
| C�� | ��X��ʾCO����ʼŨ�ȣ���Y��ʾ�Ŀ�����NO2��ת���� | |
| D�� | ��X��ʾ��Ӧʱ�䣬��Y��ʾ�Ŀ����ǻ��������ܶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
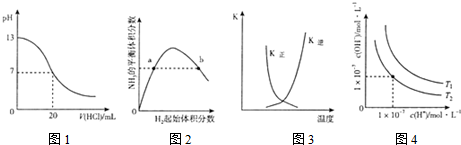
| A�� | ͼ1��ʾ25��ʱ����0��lmol L-1����ζ�20mL 0.1mol•L-1NaOH��Һ����Һ��pH�����������ı仯 | |
| B�� | ͼ2��ʾһ�������µĺϳɰ���Ӧ�У�NH3��ƽ�����������H2��ʼ���������N2����ʼ���㶨���ı仯��ͼ��a��N2��ת���ʴ���b�� | |
| C�� | ͼ3��ʾ�����ܱ������з�Ӧ��2SO2��g��+O2��g��?2SO3��g����H��0����ƽ�ⳣ��K����K�����¶ȵı仯 | |
| D�� | ͼ4��ʾ��ͬ�¶���ˮ��Һ��H+��OH-Ũ�ȵı仯�����ߣ�ͼ���¶�T2��T1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| �¶�/�� | 0 | 20 | 80 | 100 |
| �ܽ�ȣ�g/100g H2O�� | 74.4 | 91.8 | 525.8 | 535.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ���� | ��������������mL�� | NaOH��Һ��Ũ�ȣ�mol•L-1�� | �ζ����ʱ��NaOH��Һ����������mL�� |
| 1 | 20.00 | 0.10 | 24.18 |
| 2 | 20.00 | 0.10 | 23.06 |
| 3 | 20.00 | 0.10 | 22.96 |

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com