
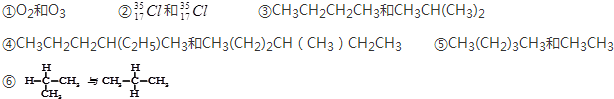
分析 质子数相同,质量数(或中子数)不同的原子互称同位素;
同种元素形成的不同单质互为同素异形体;
同系物指结构相似、通式相同,组成上相差1个或者若干个CH2原子团的化合物,官能团数目和种类相等;
具有相同分子式而结构不同的化合物互为同分异构体;
组成和结构都相同的物质为同一物质,同一物质组成、结构、性质都相同,结构式的形状及物质的聚集状态可能不同.
解答 解:①O2和O3 是由氧元素组成的不同单质,互为同素异形体;
②1735Cl和1737Cl质子数相同,中子数不同,是氯元素的不同核素,互为同位素;
③CH3CH2CH2CH3和CH3CH(CH3)2 分子式相同,结构不同,为碳链异构,互为同分异构体;
④CH3CH2CH2CH(C2H5)CH3和CH3(CH2)2CHCH3CH2CH3分子式相同,结构相同,为同一种物质;
⑤CH3(CH2)3CH3和CH3CH3结构相似,都属于烷烃,相差3个CH2原子团,互为同系物;
⑥ 名称与结构简式一致,为同一种物质;
名称与结构简式一致,为同一种物质;
故答案为:③;①;⑤;②;④⑥.
点评 本题考查同位素、同素异形体、同系物、同分异构体、同一物质的区别,难度不大,注意把握概念的内涵与外延.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:推断题
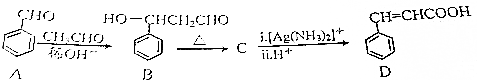
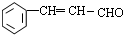 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
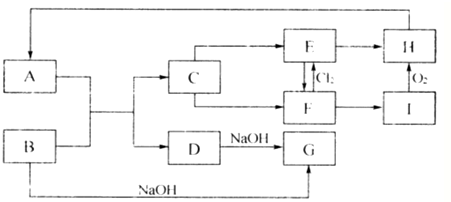
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2+HOCl→HOCH2-CH2Cl | |
| B. |  +HNO3$→_{△}^{浓硫酸}$ +HNO3$→_{△}^{浓硫酸}$ +H2O +H2O | |
| C. | 2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O | |
| D. | C12H22O11+H2O $→_{△}^{稀H_{2}SO_{4}}$ C6H12O6+C6H12O6 蔗糖 葡萄糖 果糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl、H2O、CO2、H2S | B. | Ne、NH3、P2O5、H2SO4 | ||
| C. | Na2SO4、NH4NO3、PH3、H2S | D. | Si、S、SO2、CO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O. .
. CH2OCH2CH2CHO B.
CH2OCH2CH2CHO B. CH=CHCH2CH2CHO
CH=CHCH2CH2CHO COOCH2CH2CH3 D.CH2=CHCH=CHCH=CHCH=CHCOOH.
COOCH2CH2CH3 D.CH2=CHCH=CHCH=CHCH=CHCOOH.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com