
 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可加快产生氢气的速率 | |
| B. | 对于反应2H2O2═2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 | |
| C. | 将铜片放入稀硫酸中,无现象.若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气产生 | |
| D. | 100mL 2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
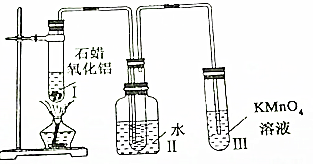
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{8}^{18}$O2-离子结构示意图: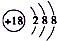 | B. | 四氯化碳分子的比例模型: | ||
| C. | 次氯酸的电子式: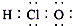 | D. | 中子数为16的硫离子:${\;}_{16}^{32}$S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
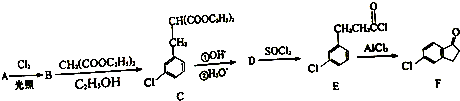
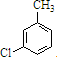 ,反应D→E的反应类型取代反应.
,反应D→E的反应类型取代反应.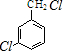 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl.
+HCl.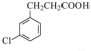 ,某化学物是D的同分异构体,能使FeCl3溶液显紫色,且分子中只有3种不同化学环境的氢,写出该化合物的结构简式:
,某化学物是D的同分异构体,能使FeCl3溶液显紫色,且分子中只有3种不同化学环境的氢,写出该化合物的结构简式: 或
或 (任写一种).
(任写一种). .
.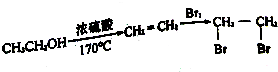
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W>R>Y>Z>X | |
| B. | X、Y和Z三种元素形成化合物中一定含有离子键和共价键 | |
| C. | 气态氢化物的稳定性:Z>Y>R | |
| D. | Y的最高价氧化物对应的水化物一定有强的氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鉴别乙醇、四氯化碳和苯可以用蒸馏水 | |
| B. | 鉴别羊毛织物和棉织物可以用灼烧并闻气味的方法 | |
| C. | 除去乙酸乙酯中含有的乙酸,最好的方法是蒸馏 | |
| D. | 鉴别甲烷、一氧化碳和氢气的方法是:点燃并先后罩上干燥的冷烧杯和涂有澄清石灰水的烧杯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com