
| A.影响反应速率大小的决定性因素是温度 |
| B.可逆反应达到化学平衡状态就是这个反应在该条件下所能达到的最大限度 |
| C.依据丁达尔效应可将分散系分为溶液、胶体与浊液 |
| D.开发海洋资源可获得Fe、Co、K、Au、Mg、B等金属 |
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源:不详 题型:单选题
 2CO △H > 0 反应速率为u1,N2+3H2
2CO △H > 0 反应速率为u1,N2+3H2 2NH3 △H<0 反应速率为u2,对于上述反应,当温度升高时,u1和u2的变化情况为
2NH3 △H<0 反应速率为u2,对于上述反应,当温度升高时,u1和u2的变化情况为| A.同时增大 | B.同时减小 | C.增大,减小 | D.减小,增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.对该反应体系加热 | B.加入硝酸铜固体 |
| C.改用粗锌 | D.不用锌片,改用锌粉 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.使用催化剂可以增大正反应速率,减小逆反应速率 |
| B.使用催化剂可以使化学平衡向正反应方向移动 |
| C.使用催化剂可以降低反应的活化能 |
| D.使用催化剂可以改变反应的平衡常数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
实验序号 | 金属 质量/g | 金属状态 | c(H2SO4) /mol·L-1 | V(H2SO4) /mL | 溶液温度/℃ | 金属消失的时间/s | |
反应前 | 反应后 | ||||||
1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
9 | 0.10 | 丝 | 1.1 | 50 | 30 | 44 | 40 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


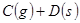 正反应速率加快的是( )
正反应速率加快的是( )| A.减少C或D的物质的量 | B.体积不变充入氦气使压强增大 |
| C.减少B的物质的量 | D.增大A或B的物质的量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.减小容器体积使压强变大 | B.恒容下,充入Ne |
| C.恒压下,充入Ne | D.恒容下,添加C(s) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.①④ | C.②③ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.2NO+O2  2NO2 2NO2 | B.N2O4 2NO2 2NO2 |
C.Br2(g)+H2 2HBr 2HBr | D.6NO+4NH3 5N2+3H2O 5N2+3H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com