
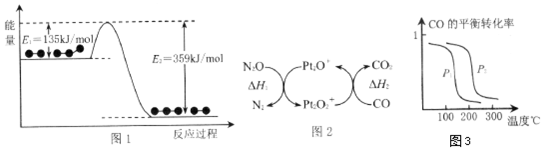
·ÖĪö £Ø1£©¢Ł·“Ó¦ĪļÄÜĮæøßÓŚÉś³ÉĪļ£¬·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬·“Ó¦ģŹ±ä”÷H=Éś³ÉĪļ×ÜģŹ-·“Ó¦Īļ×ÜģŹ£»
¢ŚŅĄ¾ŻĶ¼1ŹéŠ“ČČ»Æѧ·½³ĢŹ½£¬¢ŁN2O+Pt2O+=Pt2O2++N2 ”÷H1£¬
¢ŚPt2O2++CO=Pt2O++CO2 ”÷H2£¬½įŗĻøĒĖ¹¶ØĀɼĘĖć¢Ł+¢ŚµĆµ½N2O£Øg£©+CO£Øg£©=CO2£Øg£©+N2£Øg£©£¬½įŗĻøĒĖ¹¶ØĀɼĘĖćµĆµ½ĖłŠč·“Ó¦µÄģŹ±ä£»
£Ø2£©¢Ł¼×“¼µÄŗĻ³É·“Ó¦ŹĒĘųĢåĢå»ż¼õŠ”µÄ·“Ó¦£¬ĻąĶ¬ĪĀ¶ČĻĀ£¬Ōö“óŃ¹ĒæĘ½ŗāÕżĻņŅĘ¶Æ£¬COµÄĘ½ŗā×Ŗ»ÆĀŹŌö“ó£»
¢ŚĪĀ¶ČČŻ»ż²»±ä£¬ĻņøĆĆܱÕČŻĘ÷ŌŁŌö¼Óa mol COÓė 2a mol H2£¬µČŠ§ĪŖæŖŹ¼¼ÓČė2a mol COÓė 4a mol H2£¬Ģå»żĄ©“ó1±¶£¬Ę½ŗāŗóŌö“óŃ¹Ē棬ŌŁŃ¹Ėõ»Öø“µ½ŌĄ“Ģå»ż£¬Ōö“óŃ¹ĒæĘ½ŗāĻņĢå»ż¼õŠ”µÄ·½ĻņŅĘ¶Æ£®Ę½ŗā³£ŹżÖ»ŹÜĪĀ¶ČÓ°Ļģ£¬ĪĀ¶Č²»±ä£¬Ę½ŗā³£Źż²»±ä£»
£Ø3£©CH3COO-£©ØTc£ØNa+£©£¬øł¾ŻµēŗÉŹŲŗćæɵĆc£ØOH-£©=c£ØH+£©£¬øł¾Ż“×ĖįµÄµēĄėĘ½ŗā³£Źż±ķ“ļŹ½¼°ČÜŅŗÖŠ“×Ėį”¢“×ĖįøłĄė×ÓŗĶĒāĄė×ÓÅØ¶Č½ųŠŠ¼ĘĖć£®
½ā“š ½ā£ŗ£Ø1£©¢ŁĶ¼2·ÖĪöæÉÖŖ£¬·“Ó¦ĪļÄÜĮæøßÓŚÉś³ÉĪļ£¬·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬·“Ó¦ģŹ±ä”÷H=Éś³ÉĪļ×ÜģŹ-·“Ó¦Īļ×ÜģŹ=135KJ/mol-359KJ/mol=-226KJ/mol£¬øĆ·“Ó¦Õż·“Ó¦µÄ»ī»ÆÄÜŠ”ÓŚÄę·“Ó¦µÄ»ī»ÆÄÜ£¬¹Ź“š°øĪŖ£ŗ-224KJ/mol£»Š”ÓŚ£»
¢Ś”¢¢ŁN2O+Pt2O+=Pt2O2++N2”÷H1£¬¢ŚPt2O2++CO=Pt2O++CO2”÷H2£¬
½įŗĻøĒĖ¹¶ØĀɼĘĖć¢Ł+¢ŚµĆµ½N2O£Øg£©+CO£Øg£©=CO2£Øg£©+N2£Øg£©”÷H=”÷H1+”÷H2£¬¹Ź“š°øĪŖ£ŗ”÷H=”÷H1+”÷H2£»
£Ø2£©¢Ł¼×“¼µÄŗĻ³É·“Ó¦ŹĒĘųĢåĢå»ż¼õŠ”µÄ·“Ó¦£¬ĻąĶ¬ĪĀ¶ČĻĀ£¬Ōö“óŃ¹ĒæĘ½ŗāÕżĻņŅĘ¶Æ£¬COµÄĘ½ŗā×Ŗ»ÆĀŹŌö“󣬹Ź“š°øĪŖ£ŗ£¼£»¼×“¼µÄŗĻ³É·“Ó¦ŹĒĘųĢåĢå»ż¼õŠ”µÄ·“Ó¦£¬ĻąĶ¬ĪĀ¶ČĻĀ£¬Ōö“óŃ¹ĒæĘ½ŗāÕżĻņŅĘ¶Æ£¬COµÄĘ½ŗā×Ŗ»ÆĀŹŌö“ó£»
¢ŚĪĀ¶ČČŻ»ż²»±ä£¬ĻņøĆĆܱÕČŻĘ÷ŌŁŌö¼Óa mol COÓė 2a mol H2£¬µČŠ§ĪŖæŖŹ¼¼ÓČė2a mol COÓė 4a mol H2£¬Ģå»żĄ©“ó1±¶£¬Ę½ŗāŗóŌö“óŃ¹Ē棬ŌŁŃ¹Ėõ»Öø“µ½ŌĄ“Ģå»ż£¬Ōö“óŃ¹ĒæĘ½ŗāĻņĢå»ż¼õŠ”µÄ·½ĻņŅĘ¶Æ£®øĆ·“Ó¦ĪŖĘųĢåĢå»ż¼õŠ”µÄ·“Ó¦£¬¹ŹĻņÕż·“Ó¦ŅĘ¶Æ£¬CO×Ŗ»ÆĀŹŌö“ó£®
Ę½ŗā³£ŹżÖ»ŹÜĪĀ¶ČÓ°Ļģ£¬ĪĀ¶Č²»±ä£¬Ę½ŗā³£Źż²»±ä£®
¹Ź“š°øĪŖ£ŗŌö“ó£»²»±ä£»
£Ø3£©³£ĪĀĻĀ£¬½«c1mol/LµÄCH3COOHČÜŅŗÓėc2mol/LµÄNaOHČÜŅŗµČĢå»ż»ģŗĻ£¬·“Ó¦Ę½ŗāŹ±ČÜŅŗÖŠc£ØCH3COO-£©=c£ØNa+£©=0.5c2mol/L£¬øł¾ŻµēŗÉŹŲŗćæɵĆc£ØOH-£©=c£ØH+£©£¬³£ĪĀĻĀµÄÖŠŠŌČÜŅŗÖŠc£ØOH-£©=c£ØH+£©=10-7mol/L£¬c£ØCH3COOH£©=0.5£Øc1mo/L-c2mol/L£©£¬“×ĖįµÄµēĄėĘ½ŗā³£ŹżĪŖ£ŗK=$\frac{c£Ø{H}^{+}£©•c£ØC{H}_{3}CO{O}^{-}£©}{c£ØC{H}_{3}COOH£©}$=$\frac{1{0}^{-7}{c}_{2}}{{c}_{1}-{c}_{2}}$£¬¹Ź“š°øĪŖ$\frac{1{0}^{-7}{c}_{2}}{{c}_{1}-{c}_{2}}$£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ·“Ó¦ÄÜĮæ±ä»Æ”¢Ķ¼Ļó·ÖĪö”¢øĒĖ¹¶ØĀɵĥķ½āÓ¦ÓĆ”¢Ę½ŗā¼ĘĖćÓėŅĘ¶Æ”¢Ę½ŗā³£ŹżµČÖŖŹ¶£¬×¢Ņā·“Ó¦»ī»ÆÄÜµÄ“óŠ”±Č½Ļ£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 4.08gĆ¾ĀĮŗĻ½šÖŠŗ¬ÓŠĆ¾ŗĶĀĮµÄÖŹĮæ·Ö±šĪŖ1.92g”¢2.16g | |
| B£® | Éś³É³ĮµķµÄ×ī“óÖŹĮæĪŖ10.88g | |
| C£® | Čō°×É«³ĮµķÖ»ÓŠMg£ØOH£©2£¬øĆNaOHČÜŅŗµÄÅضČÖĮÉŁĪŖ0.96mol/L | |
| D£® | Čܽā4.08 gĆ¾ĀĮŗĻ½šŹ±£¬Ź£ÓąŃĪĖįµÄĪļÖŹµÄĮæĪŖ0.1 mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·“Ó¦µōµÄČżÖÖ½šŹōµÄÖŹĮæĻąµČ | B£® | ·“Ó¦ŗóČżÖÖ½šŹōÖŹĮæĻąµČ | ||
| C£® | ĖłÓĆŃĪĖį¾ł¹żĮæ | D£® | ČżÖÖ½šŹōæÉŅŌ¶¼ÓŠŹ£Óą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚÕōĮóÉÕĘæÖŠŹ¢Ō¼$\frac{1}{3}$Ģå»żµÄ×ŌĄ“Ė®£¬²¢·ÅČė¼øĮ£·ŠŹÆ[KS5UKS5U] | |
| B£® | æÉŅŌ²»ÓĆĪĀ¶Č¼Ę | |
| C£® | ĄäĖ®“ÓĄäÄż¹ÜÉĻæŚČė£¬ĻĀæŚ³ö | |
| D£® | ȔɣĮæŹÕ¼Æµ½µÄŅŗĢåµĪČėĻõĖįŅųŗĶĻ”ĻõĖį£¬ĪŽĆ÷ĻŌĻÖĻó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | CO2 | B£® | H2O | C£® | CO | D£® | CCl4 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com