
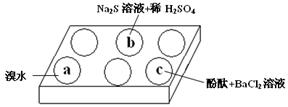
| 编号 | 实验现象 |
| a | 溴水褪色 |
| b | 产生淡黄色沉淀 |
| c | 滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去 |
| n(SO32—): n(HSO3—) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
 HSO3-+OH-,所以滴入酚酞后溶液变红;在该溶液中加入BaCl2后,Ba2++SO32-=BaSO3↓(白色),由于c(SO32-)减小,SO32-水解平衡左移,c(OH-)减小,红色褪去。(2分)
HSO3-+OH-,所以滴入酚酞后溶液变红;在该溶液中加入BaCl2后,Ba2++SO32-=BaSO3↓(白色),由于c(SO32-)减小,SO32-水解平衡左移,c(OH-)减小,红色褪去。(2分) HSO3-+OH-,所以滴入酚酞后溶液变红;在该溶液中加入BaCl2后,Ba2++SO32-=BaSO3↓(白色),由于c(SO32-)减小,SO32-水解平衡左移,c(OH-)减小,红色褪去。(2分)
HSO3-+OH-,所以滴入酚酞后溶液变红;在该溶液中加入BaCl2后,Ba2++SO32-=BaSO3↓(白色),由于c(SO32-)减小,SO32-水解平衡左移,c(OH-)减小,红色褪去。(2分)

科目:高中化学 来源:不详 题型:填空题
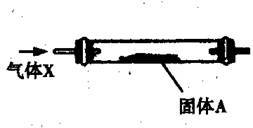
| A.固体A为无水硫酸铜时,可以检验气体X中是否含有水蒸气 |
| B.固体A为铜时,可以除去N2中的O2 |
| C.在空气流作用下,加热氯化铁晶体得到纯净的无水氯化铁 |
| D.将氨气和空气混合气通过灼热的铂丝,可看到有红棕色气体生成 |
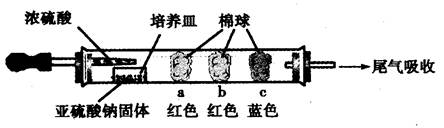
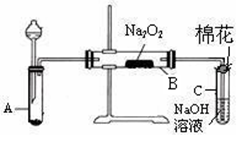
| 棉球 | 棉球上滴加的试剂 | 实验现象 | 解释和结论 |
| a | | 棉球变白,微热后又恢复红色 | |
| b | 含酚酞的NaOH溶液 | 棉球变为白色 | 离子方程式: |
| c | | 棉球变为白色 | 结论:该气体具有 性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
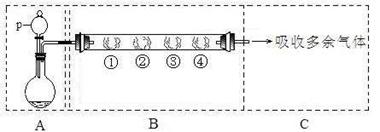
| B中棉花的位置 | ① | ② | ③ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 碘水(黄色) |
| 现象 | | 褪色 | |
| 体现SO2的性质 | 水溶液显酸性 | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.FeS和CuS | B.CuS | C.CuS和S | D.Al2S3、FeS和CuS |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

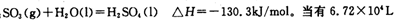 (已折算为标况下)SO3气体与H2O化合时放出的热量为 (保留两位有效数字)。
(已折算为标况下)SO3气体与H2O化合时放出的热量为 (保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓硫酸能将炽热的木炭氧化为二氧化碳 |
| B.稀硫酸能按水的组成比脱去蔗糖中的氢、氧元素 |
| C.硫酸和硝酸分别与金属反应时,S和N元素的化合价一定发生变化 |
| D.因为浓硫酸或浓硝酸能与铝反应,所以常温下二者都不能用铝制容器盛装 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓硫酸能与灼热的木炭反应,生成二氧化碳和二氧化硫 |
| B.浓硫酸具有吸水性,在实验室中常用作干燥剂 |
| C.常温下,可以用铁质或铝质容器储存浓硫酸或浓硝酸 |
| D.浓硫酸与铜反应产生的气体对环境无影响 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铵盐热分解一定有氨气产生。 |
| B.因为SO2可以使酸性KMnO4溶液褪色,所以SO2有漂白性; |
| C.二氧化硫和二氧化氮都能形成酸雨,酸雨的pH<5.6; |
| D.用铜和稀硝酸反应制取NO,并用向上排空气法收集气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com