

| A. | 甲池通入O2的电极反应为O2+4e-+4H+=2H2O | |
| B. | 乙池 Ag电极增重6.4g,溶液中将转移0.2mol电子 | |
| C. | 反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度 | |
| D. | 甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体 |
分析 A、电解质溶液为KOH;
B、电解质溶液中没有电子转移;
C、电解池中,电解后的溶液复原遵循:出什么加什么的思想;
D、根据串联电路中转移电子相等结合电子守恒知识来回答.
解答 解:A、电解质溶液为KOH,通入O2的电极反应为O2+4e-+2H2O=4OH-,故A错误;
B、电解质溶液中没有电子转移,是离子定向移动,故B错误;
C、电解池乙池中,电解后生成硫酸、铜和氧气,要想复原,要加入氧化铜,故C错误;
D、甲池中根据电极反应:O2+2H2O+4e-=4OH-,所以消耗280mL(标准状况下0.0125mol)O2,则转移电子0.05mol,根据丙装置中,在阴极上是氢离子放电,转移电子0.05mol,减小的氢离子是0.05mol,氢氧根离子是0.05mol,镁离子和氢氧根离子之间反应生成氢氧化镁,理论上最多产生氢氧化镁质量应该是0.05mol×$\frac{1}{2}$×58g/mol=1.45g固体,故D正确.
故选D.
点评 本题考查学生原电池和电解池的工作原理知识,属于综合知识的考查,注意平时知识的积累是解题的关键,难度较大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 两烧杯中铜片表面均无气泡产生 | B. | 甲中化学能转化成了电能 | ||
| C. | 甲中铜片是负极 | D. | 乙中铜片是正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中:Al3+、NH4+、Cl-、HCO3- | |
| B. | 甲基橙显红色的溶液中:Fe2+、Na+、SO42-、NO3- | |
| C. | 水电离出来的c(H+)=10-12mol•L-1的溶液:K+、HCO3-、I-、ClO- | |
| D. | pH值为1的溶液:Fe2+、Cl-、Na+、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将lmol Cl2溶于水,所得溶液中HClO、Cl-和C1O-的总数目为2NA | |
| B. | 46g NO2和N2O4混合物中含分子数为NA | |
| C. | 氢氧燃料电池正极消耗22.4L气体时,电路中通过的电子数目为4NA | |
| D. | 适量Na2O2与CO2反应生成1mol O2时,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a+m=b-n | B. | a+b=m+n | C. | a-m=b+n | D. | a+m=b-n |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含质子数=A-n | B. | 所含中子数=A-Z | C. | 所含电子数=Z+n | D. | 质量数=A+Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6-2 | +5-3 | -2 | +3 |
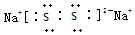 ;所含化学键类型离子键、共价键.
;所含化学键类型离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 时间 | 开始 | 8h后 | 16h 后 | 24h后 | 32h后 | 40h后 | 48h后 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com