
在学习了铜元素的性质之后,小明同学做了H2O2与铜的有关探究实验:
实验一:将铜丝置于装有H2O2溶液的试管中,没有气体产生;加热溶液时,观察到铜丝表面产生大量气体。
实验二:将铜丝置于装有硫酸酸化的H2O2溶液的试管中,溶液迅速变蓝。同时产生大量气体。
请回答下列问题:
(1)上述实验一(加热时)、实验二中铜丝表面均产生了大量气体,该气体是 。
(2)写出在酸性条件下H2O2氧化铜丝的离子方程式: 。
(3)H2O2能发生多种化学反应,等物质的量的H2O2在仅作氧化剂的反应、仅作还原剂的反应和分解反应中转移的电子数目之比为 。
小明同学设计了以废铜屑制取硫酸铜的三个方案:

①认为最佳方案是 。
②简述另两个方案的不足之处: 。
(1)O2(2分)
(2)H2O2+2H++Cu=Cu2++2H2O(2分)
(3)2∶2∶1(2分)
(4)①方案二(1分)
②方案一生成的二氧化硫污染环境的同时会消耗更多的硫酸,方案三铜会催化过氧化氢的分解,增大成本(2分)
【解析】
试题分析:(1)结合题意分析可知为:O2。
(2)H2O2+2H++Cu=Cu2++2H2O
(3)H2O2在仅作氧化剂的反应中-1价氧转变为-2价氧的得2电子、仅作还原剂的反应-1价氧转变为0价氧失去2电子,分解反应中-1价氧转移的1电子,等物质的量H2O2转移的数目之比为2∶2∶1。
(4)方案一生成的二氧化硫污染环境的同时会消耗更多的硫酸,方案三铜会催化过氧化氢的分解,增大成本,所以选择方案二。
考点:考察元素及其化合物性质、化学反应的计算。


科目:高中化学 来源: 题型:阅读理解
| 实验内容 | 实验操作 | 实验现象 | 推断生成物 |
| 氯气与铁反应 | |||
| 氯气与氢气反应 | |||
| 氯气与碘化钾溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
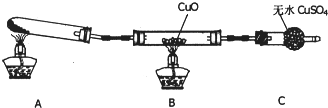
| H+ |
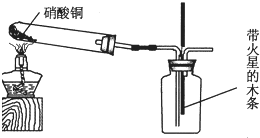
查看答案和解析>>
科目:高中化学 来源:09-10学年衡中高一下学期第二次调研化学试卷 题型:实验题
(10分)Ⅰ: 元素的金属活动性递变规律是元素周期表学习的重要内容之一。某校研究性学习小组查阅课外资料,看到第IVA族的三种金属锗、锡、铅的性质:“锗、锡在空气中不反应,铅在空气中表面生成一层氧化铅,请解释发生上述变化的原因是
。
Ⅱ: 另一研究性学习小组欲通过实验探究Zn、Fe、Cu的金属活动性顺序,根据不同的实验条件设计了如下的几种实验方案:
(1)该小组同学根据提供的Zn片、Fe片和稀硫酸,设计成了一个原电池比较锌与铁的活动性顺序,请在下侧方框内画出原电池装置图。并写出正极的反应现象及电极反应式。
现象 ;电极反应式 。

(2)现只有Fe片、CuO和稀硫酸这几种药品,请你帮忙设计方案比较铁与铜的活动性顺序。你的设计方法是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com