
【题目】海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行以下实验:

请填写下列空白:
(1)CCl4是____色、比水____的液体。步骤⑤后静置,下层液体的颜色为______色,上层液体的成分为___________。该步骤所用主要玻璃仪器的名称是__________。
(2)能选用CCl4获取碘的原因是_____________________、___________________、_______
【答案】无色 密度大 紫红色(或紫色) MnSO4、K2SO4 分液漏斗 有机溶剂CCl4溶解碘的能力大于水 CCl4难溶于水 CCl4与水不反应
【解析】
实验室从海带中提取碘:海带灼烧①成海带灰,浸泡②溶解得到海带灰悬浊液,通过过滤③,得到不溶的残渣和含碘离子的滤液,向含碘离子的滤液中加入稀硫酸、氧化剂MnO2④,将碘离子氧化成碘单质,反应为MnO2+2KI+2H2SO4═MnSO4+K2SO4+2H2O+I2,利用有机溶剂CCl4萃取⑤出碘水中碘单质得到碘的四氯化碳溶液,再通过蒸馏⑥提取出碘单质,据此分析解答。
(1)四氯化碳是一种有机溶剂,是一种无色液体,密度大于水,碘易溶于有机溶剂,从碘水中提取碘可以用有机溶剂萃取然后分液;所以操作⑤为萃取、分液,所用仪器为分液漏斗,碘溶于四氯化碳中,下层液体是紫红色(或紫色),含碘离子的溶液加入二氧化锰和稀硫酸,碘离子被氧化为碘单质,得到含碘水溶液,反应为MnO2+2KI+2H2SO4═MnSO4+K2SO4+2H2O+I2,上层溶液中含有MnSO4和K2SO4;
(2)有机溶剂CCl4溶解I2的能力大于水,并且难溶于水,又与水不反应,故可以作CCl4获取碘。


科目:高中化学 来源: 题型:
【题目】(1)FeCl3溶液呈_______性,原因是__________(用离子方程式表示)。把FeCl3溶液蒸干后并灼烧,最后得到的主要固体产物是_________。
(2)在25℃下,将a mol·L-1的CH3COOH与0.01 mol·L-1的NaOH等体积混合,反应平衡时溶液中c(CH3COO-)=c(Na+),则溶液显______ (填“酸”、“碱”或“中”)性;用含a的代数式表示CH3COOH的电离常数Ka=__________ 。
(3)已知298 K和101 kPa条件下:
N2(g)+3H2(g)=2NH3(g) ΔH1
2H2(g)+O2(g)=2H2O(l) ΔH2
2H2(g)+O2(g)=2H2O(g) ΔH3
4NH3(g)+O2(g)=2N2H4(l)+2H2O(l) ΔH4
则N2H4(l)的标准燃烧热ΔH=_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】薄荷油中含有少量的α—非兰烃和β—非兰烃,两者互为同分异构体,其相对分子质量为136。根据如下化学转化,回答相关问题:

已知: +R’CO2H
+R’CO2H
 +CO2
+CO2
(1)分别写出C→D和D→E的反应类型:___;___。
(2)写出B、F、H、β—非兰烃的结构简式:B:___;F:___;H:___;β—非兰烃:___。
(3)A的同分异构体中含有两个—COOCH3基团的化合物共有___种(不考虑手性异构),其中核磁共振氢谱呈现2个吸收峰的异构体结构简式为___。
(4)α—非兰烃与等物质的量的Br2进行加成反应的产物共有___种(不考虑立体异构)。
(5)写出C→M反应的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用右图所示装置进行下列实验,能得出相应实验结论的是( )
选项 | ① | ② | ③ | 实验结论 | 实验装置 |
A | 稀硫酸 | Na2S | AgNO3与AgCl的溶液 | Ksp(AgCl)>Ksp(Ag2S) |
|
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性钡盐均可以生成白色沉淀 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究性学习小组用Na2SO3与硫酸溶液(硫酸与水体积比1∶1)制备SO2并进行性质探究实验。

(1)D中的实验现象是_____________,C、E中溶液都褪色,分别体现SO2________、_______性质。
(2)请在方框中画出收集SO2以及尾气处理装置(标相关试剂)。___________
(3)研究小组发现B中有白色沉淀,为了清楚沉淀的物质,研究小组往B中加入过量稀盐酸,沉淀 不溶解,你认为留下的沉淀物是__________,形成该沉淀的反应方程式有:_________________________________________________________________________________
为了进一步验证沉淀原因,研究小组另取BaC12溶液,加热煮沸,冷却及 时加入少量苯液封,然后再通SO2,结果发现沉淀量减少,但仍有轻微浑 浊。研究小组改进A装置(如图),再进行实验,B中没有出现浑浊。下列气体可作为X气体的是_____________

A.CO2 B.NH3 C.O3 D.N2 E.NO2
(4)SO2为空气污染物,研究小组为测定某工厂区空气中SO2的含量,取10m3(标准状况)的空气, 缓慢通过足量溴水中,在所得溶液中加入过量的BaC12溶液,将产生的白色沉淀洗涤、干燥,用电子称称其质量为0.233g,则:
① 检验洗涤已经干净的实验操作是_________________________________________________。
② 试计算此空气中SO2的浓度(列出计算表达式并计算结果,结果单位用mg/m3表示)。________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷(![]() )是最简单的一种。下列关于该化合物的说法错误的是
)是最简单的一种。下列关于该化合物的说法错误的是
A. 与环戊烯互为同分异构体
B. 二氯代物超过两种
C. 所有碳原子均处同一平面
D. 生成1 molC5H12至少需要2 molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化妆品的组分Z具有美白功效,原从杨树中提取,现可用如下反应制备:

下列叙述错误的是
A. X、Y和Z均能使溴水褪色
B. X和Z均能与NaHCO3溶液反应放出CO2
C. Y既能发生取代反应,也能发生加成反应
D. Y可作加聚反应单体,X可作缩聚反应单体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量相同的NaHCO3和KHCO3固体混合物9.20g与0.2mol/L盐酸反应。
(1)欲求标准状况下生成CO2的体积,还需要什么数据___。(讨论(2)的问题中,该数据用a表示)
a | 生成CO2的体积(L) |
(2)讨论a值的变化时,产生CO2的体积(标准状况)___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S存在于多种燃气中,脱除燃气中H2S的方法很多。

(1) 2019年3月《science direct》介绍的化学链技术脱除H2S的原理如图所示。
①“H2S氧化”反应中氧化剂与还原剂的物质的量之比为________。
②“HI分解”时,每1 mol HI分解生成碘蒸气和氢气时,吸收13 kJ的热量,写出该反应的热化学方程式:________。
③“Bunsen反应”的离子方程式为________。
(2) 电化学干法氧化法脱除H2S的原理如图所示。阳极发生的电极反应为________;阴极上COS发生的电极反应为________。

(3) 用Fe2(SO4)3吸收液脱除H2S法包含的反应如下:
(Ⅰ) H2S(g)![]() H2S(aq)
H2S(aq)
(Ⅱ) H2S(aq) ![]() H++HS-
H++HS-
(Ⅲ) HS-+2Fe3+=S↓+2Fe2++H+
一定条件下测得脱硫率与Fe3+浓度的关系如图所示。
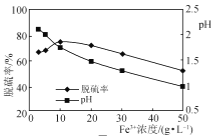
①吸收液经过滤出S后,滤液需进行再生,较经济的再生方法是________。
②图中当Fe3+的浓度大于10 g·L-1时,浓度越大,脱硫率越低,这是由于________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com