
ij�о���ѧϰС���������²�����̽��NH3�Ļ�ԭ�ԣ�����ʵ��װ������ͼ��
����1��NH3��ǿ��ԭ�����ܽ�ijЩ���������ﻹԭΪ�������ʻ�ͼ�̬��������磺
2NH3 + 3CuO  3Cu + N2 +3H2O
3Cu + N2 +3H2O
����2��Cu+��������Һ�в��ȶ����ɷ�������������ԭ��Ӧ����Cu2O����ɫ��������Cu2+��Cu��
Cu2O + 2H+ ="=" Cu2+ + Cu +H2O
��ش��������⣺
(1)Ϊ֤��NH3��ԭCuO�ķ�Ӧ����ˮ���ɣ�B��Ӧ������Լ��� ��
(2)���۲쵽 ��������������A�еķ�Ӧ�Ѿ���ɣ�
(3)��С�����������Ϊ1�U4��ϡ�������Լ������鷴Ӧ�Ƿ���Cu2O�������ɡ�����98%��Ũ��������1�U4��ϡ���ᣬ����IJ����������˽�ͷ�ι���� ��
(4)��֤����ԭ�����к���Cu2O�IJ����������� ��
(5)��д��A������Cu2O�Ļ�ѧ����ʽ ��
(6)���ö����ķ����ⶨ�÷�Ӧ�Ƿ�����Cu2O��������ȷ�ķ�����
��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ����� | 1 | 2 | 3 |
| KI��Һ���/mL | 19.98 | 20.02 | 20.00 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| �� |
| �� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
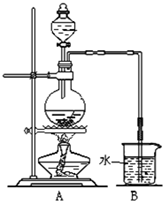 ��ͼ��ij�о���ѧϰС������ʵ������������װ�������ȡ��ˮ���������ʵ�飮
��ͼ��ij�о���ѧϰС������ʵ������������װ�������ȡ��ˮ���������ʵ�飮
| ||
| ||
 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| 1 |
| 2 |
| 1 |
| 2 |
| ||
. |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
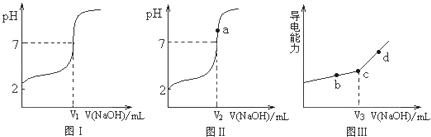
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com