
【题目】下列有关卤族元素的说法中,正确的是 ( )
A. 原子半径:F>C1>Br>IB. 最外层电子数:F>C1>Br>I
C. 熔、沸点:F2>Cl2>Br2>I2D. 热稳定性:HF>HCl>HBr>HI
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1molL﹣1的三种酸(HA、HB和HD)溶液,滴定曲线如图所示,下列判断错误的是( ) 
A.三种酸的电离常数关系:KHA>KHB>KHD
B.滴定至P点时,溶液中:c(B﹣)>c(Na+)>c(HB)>c(H+)>c(OH﹣)
C.pH=7时,三种溶液中:c(A﹣)=c(B﹣)=c(D﹣)
D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH﹣)﹣c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下将0.1mol N2和0.3mol H2置于密闭容器中发生反应:N2+3H2 ![]() 2NH3 . 下列关于该反应的说法正确的是( )
2NH3 . 下列关于该反应的说法正确的是( )
A.最终可生成0.2 mol NH3
B.增大压强能使反应速率减小
C.降低反应体系的温度能加快反应速率
D.向容器中再加入N2 , 能加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质与用途具有对应关系的是( )
A. Al2O3熔点高,可用作耐高温材料
B. SO2具有氧化性,可用于漂白纸浆
C. SiO2硬度大,可用于制造光导纤维
D. NH3易溶于水,可用作制冷剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,可形成氢氧燃料电池.通常氢氧燃料电池有酸式(当电解质溶液为硫酸时)和碱式[当电解质溶液为NaOH(aq)或KOH(aq)时]两种.试回答下列问题: 
(1)酸式电池的电极反应:负极 , 正极;电池总反应:;电解质溶液pH的变化(填“变大”“变小”或“不变”).
(2)碱式电池的电极反应:负极 , 正极;电池总反应:;电解质溶液pH的变化(填“变大”“变小”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期元素,Y、Z同周期且相邻,X、W同主族且与Y处于不同周期,Y、Z原子的电子数总和与X、W原子的电子数总和之比为5:4,下列说法正确的是( )
A.原子半径:r(W)>r(Z)>r(Y)>r(X)
B.Y的简单气态氢化物的热稳定性比Z的强
C.由X、Z组成的化合物与由Z、W组成的化合物只能发生化合反应
D.由X、Y、Z三种元素组成的化合物可以是酸、碱或盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.
(1)X与Y所形成化合物晶体的晶胞如图所示.在1个晶胞中,X离子的数目为 .
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是 .
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是 .
(4)Y与Z可形成YZ42﹣ , YZ42﹣的空间构型为(用文字描述);写出一种与YZ42﹣互为等电子体的分子的化学式: . 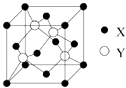
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.H2O(g)=H2O(l)△H=﹣44kJ/mol,所以该过程是放热反应
B.人类利用的能源都是通过化学反应获得的
C.2CO(g)+O2 ![]() 2CO2(g)△H<0,则56gCO和32gO2所具有的总能里大于88g所具有的总能量
2CO2(g)△H<0,则56gCO和32gO2所具有的总能里大于88g所具有的总能量
D.需要加热的反应一定是吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com