
| A、燃烧时有浓厚的黑烟 |
| B、实验室制乙炔时可用CuSO4除杂质气体 |
| C、为了减缓电石和水的反应速率,可用饱和食盐水来代替 |
| D、乙炔的收集方法可用排空气法收集 |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 水解反应(取代反应)A、B、C、D均为含苯环的有机物,且相对分子质量B>A>C.已知有机物A的结构简式为
水解反应(取代反应)A、B、C、D均为含苯环的有机物,且相对分子质量B>A>C.已知有机物A的结构简式为
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 和
和 .下列各物质中,能形成类似上述两种空间异构体的是( )
.下列各物质中,能形成类似上述两种空间异构体的是( )| A、1,1-二氯乙烯 |
| B、2-甲基-2-戊烯 |
| C、3-甲基-2-戊烯 |
| D、1-戊烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某期刊封面上有如下一个常见分子的球棍模型图图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,该模型图代表的有机物中含有的官能团是( )
某期刊封面上有如下一个常见分子的球棍模型图图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,该模型图代表的有机物中含有的官能团是( )| A、氨基和羧基 |
| B、碳碳双键和羧基 |
| C、碳碳双键和羟基 |
| D、氨基和醛基 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、该反应的反应过程与能量关系可以用图表示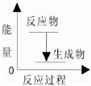 |
| B、若将该反应设计成原电池,当正极产生22.4L气体时,有56g铁溶解 |
| C、若将该反应设计成原电池,溶液中SO42-向Fe电极移动 |
| D、若将该反应设计成原电池,负极发生的反应是:Fe-2e=Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com