
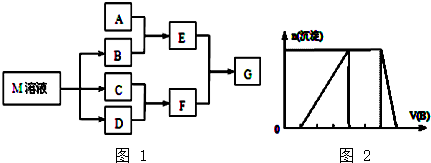
分析 (1)C可在D中燃烧发出苍白色火焰,为氢气与氯气反应生成HCl,可推知C为H2、D为Cl2、F为HCl,M是日常生活中不可缺少的调味品,由转化关系可知,M的溶液电解生成氢气、氯气与B,可推知M为NaCl、B为NaOH,
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,则A为SiO2,E为Na2SiO3,与F溶液反应可以制备G为H2SiO3;
(3)若A是一种常见金属单质,且与NaOH溶液能够反应,则A为Al,E为NaAlO2,则将过量的HCl溶液逐滴加入NaAlO2溶液中,先生成氢氧化铝,而后氢氧化铝溶解;
(4)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,可推知A中含有Fe2+,E为Fe(OH)3,G为FeCl3;
(5)若A是一种化肥,实验室可用A和NaOH反应制取气体E,则E为NH3、A为铵盐,E与氯气相遇均冒白烟,且利用E与氯气的反应检验输送氯气的管道是否泄露,则氨气与氯气反应生成氯化铵,同时生成氮气;
(6)由图可知,开始加入NaOH没有沉淀和气体产生,则一定有H+,一定没有CO32-,后来有沉淀产生且最后消失,则一定没有Mg2+、Fe3+,一定含有Al3+;中间段沉淀的质量不变,应为NH4++OH-=NH3•H2O的反应,则含有NH4+,由电荷守恒可知一定含有SO42-.
解答 解:(1)C可在D中燃烧发出苍白色火焰,为氢气与氯气反应生成HCl,可推知C为H2、D为Cl2、F为HCl,M是日常生活中不可缺少的调味品,由转化关系可知,M的溶液电解生成氢气、氯气与B,可推知M为NaCl、B为NaOH,用惰性电极电解M溶液的离子方程式为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑,
故答案为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑;
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,则A为SiO2,E为Na2SiO3,与F溶液反应可以制备G为H2SiO3,E的溶液俗称水玻璃,
故答案为:水玻璃;
(3)若A是一种常见金属单质,且与NaOH溶液能够反应,则A为Al,E为NaAlO2,则将过量的HCl溶液逐滴加入NaAlO2溶液中,先生成氢氧化铝,而后氢氧化铝溶解,故看到的现象为:溶液中逐渐有白色絮状沉淀生成,且不断增加;然后又由多到少,最后消失,
故答案为:溶液中逐渐有白色絮状沉淀生成,且不断增加;然后又由多到少,最后消失;
(4)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,可推知A中含有Fe2+,E为Fe(OH)3,G为FeCl3,则由A转化成E的离子方程式是:4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓,
故答案为:4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓;
(5)若A是一种化肥,实验室可用A和NaOH反应制取气体E,则E为NH3、A为铵盐,E与氯气相遇均冒白烟,且利用E与氯气的反应检验输送氯气的管道是否泄露,则氨气与氯气反应生成氯化铵,同时生成氮气,反应方程式为:3Cl2+8NH3=N2+6NH4Cl,
故答案为:3Cl2+8NH3=N2+6NH4Cl;
(6)由图可知,开始加入NaOH没有沉淀和气体产生,则一定有H+,一定没有CO32-,后来有沉淀产生且最后消失,则一定没有Mg2+、Fe3+,一定含有Al3+;中间段沉淀的质量不变,应为NH4++OH-=NH3•H2O的反应,则含有NH4+,由电荷守恒可知一定含有SO42-,
故答案为:NH4+、SO42.
点评 本题考查无机物推断等,题目涉及元素化合物较多,需要学生全面掌握据基础知识,(6)中根据图象中的平台确定含有铵根离子是关键,注意电荷守恒的应用,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 铜能导电,所以铜是电解质 | |
| B. | BaSO4难溶于水,所以BaSO4属于非电解质 | |
| C. | 虽然液态HCl不能导电,但HCl的水溶液能导电,所以HCl是电解质 | |
| D. | 氯气的水溶液能导电,氯气是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向含3mol次氯酸钠溶液中通入1mol二氧化硫:3ClO-+H2O+SO2═2HClO+SO4-+Cl- | |
| B. | 向碳酸氢钠溶液中加入过量氢氧化钙溶液2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| C. | 氢氧化钡溶液与硫酸溶液反应得到中性溶液Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 50mL1mol/L的FeI2溶液中通入0.05molCl2:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO4在熔融状态下的电离方程式为NaHSO4═Na++H++SO42- | |
| B. | H2CO3是弱酸,故Na2CO3是弱电解质 | |
| C. | Fe3O4俗称铁红,常用作红色油漆和涂料 | |
| D. | 2.4 g Mg无论与O2还是与N2完全反应转移的电子数均为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LCH2Cl2中含有C-Cl键数目为0.2NA | |
| B. | 常温常压下,3.0g尿素与乙酸的混合物,含氢原子总数为0.2NA | |
| C. | 常温常压下,10g92%酒精水溶液含氧原子总数为0.2NA | |
| D. | 常温常压下,0.1molNa2O2与水完全反应转移电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M与X可形成两种常见的共价化合物,与W可形成两种常见的离子化合物 | |
| B. | Y的氢化物的沸点低于Z的氢化物的沸点 | |
| C. | Z的氢化物结合H+的能力强于M的氢化物结合H+的能力 | |
| D. | Z、M、W形成的简单离子,其半径大小W>Z>M |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①=④>③=② | B. | ①=④>③>② | C. | ①>④>③>② | D. | ④>①>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
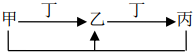 甲、乙、丙、丁四种物质中,甲、乙、丙含有相同的某种元素,它们之间有如下转化关系,则下列有关物质的推断错误的是( )
甲、乙、丙、丁四种物质中,甲、乙、丙含有相同的某种元素,它们之间有如下转化关系,则下列有关物质的推断错误的是( )| A. | 若甲为焦炭,则丁可能是O2 | |
| B. | 若甲为NaOH溶液,则丁可能是CO2 | |
| C. | 若甲为铝盐溶液,则丁可能是NaOH溶液 | |
| D. | 若甲为Fe,则丁可能是氯气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com