
科目:高中化学 来源:2014-2015学年山东济南外国语学校高一上期中化学试卷(解析版) 题型:选择题
下列离子方程式的写法正确的是:
A.单质钠与水的反应:Na+H2O==Na++OH-+H2↑
B.氢气在氯气中燃烧:H2+Cl2==2H++2Cl-
C.小苏打治疗胃酸过多:H++ HCO3-==H2O+CO2↑
D.用氯化铁溶液腐蚀铜箔制造印刷电路板:Fe3++Cu==Fe2++Cu2+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁育才学校高一上第一次阶段测化学试卷(解析版) 题型:实验题
CO、CH4均为常见的可燃性气体。120℃、101 kPa下,a mL由CO、CH4组成的混合气体在bmL O2中完全燃烧后,恢复到原温度和压强。
(1)若混合气体与氧气恰好完全反应,产生bmL二氧化碳,混合气体中一氧化碳和甲烷的物质的量之比为: 。
(2)若燃烧后气体体积缩小了a/4 mL,则a与b关系的数学表示式是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁师大附属中学高二10月月考化学试卷(解析版) 题型:填空题
(13分)研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)已知石墨的标准燃烧热为y kJ·mol-1,1.2g石墨在1.68L(标准状况)氧气中燃烧,至反应物耗尽,放出x kJ热量,则石墨与氧气反应生成CO的热化学方程式为________________。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H
CH3OH(g)+H2O(g) △H

①该反应的平衡常数表达式为K=______________________。
②取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图2所示,则上述CO2转化为甲醇反应的ΔH_______________(填“>” “<”或“=”)0。
③在两种不同温度下发生反应,测得CH3OH的物质的量随时间变化如图3所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ____________KⅡ(填“>” “<”或“=”)。
④一定温度下,在容积相同且固定的两个密闭容器中,按如下方式投入反应物,一段时间后达到平衡。
容 器 | 甲 | 乙 |
反应物 投入量 | 1molCO2 3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) (a、b、c均不等于0) |
若甲中平衡后气体的压强为开始时的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持反应逆向进行,则c的取值范围为________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东寿光中学高二上10月月考化学试卷(解析版) 题型:填空题
(10分)I、在理论上不能用于设计原电池的化学反应是
A.CH4(g)+2 O2(g)= C O2(g)+2 H2O(1) △H <0
B.Ba(OH)2·8H2O(s)+2NH4Cl(s)= BaCl2(aq)+2NH3·H2O(aq)+8H2O(1) △H >0
C.4Al(s)+ 6H2O(1)+ 3O2(g)==4Al(OH)3(s) △H <0
D.Zn(s)+2MnO2(s)+2H2O(1)= 2MnOOH(s)+Zn(OH)2(s) △H <0
若你认为A可以设计成原电池,创造碱性环境,请写出负极的电极反应式为 (若你认为不能此空不填)。
II、北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)
(1)丙烷脱氢可得丙烯。
已知:C3H8(g) = CH4(g)+HC CH(g)+H2(g) △H1=156.6 kJ·mol-1
CH(g)+H2(g) △H1=156.6 kJ·mol-1
CH3CH CH2(g) = CH4(g)+HC
CH2(g) = CH4(g)+HC CH(g ) △H2=32.4 kJ·mol-1
CH(g ) △H2=32.4 kJ·mol-1
则相同条件下,反应C3H8(g)= CH3CH CH2(g)+H2(g)的△H= kJ·mol-1。
CH2(g)+H2(g)的△H= kJ·mol-1。
(2)以丙烷为燃料制作燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为 ;放电时CO32-移向电池的 (填“正”或“负”)极。负极的电极反应式为 w.w.w.k.s.5.u.c.o.m
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东寿光中学高一上10月月考化学试卷(解析版) 题型:选择题
1g N2中含有n个N2的分子,则阿伏加德罗常数(NA)可以表示为
A.14n mol-1 B.28n mol-1 C.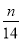 mol-1 D.
mol-1 D.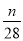 mol-1
mol-1
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期四调考试化学试卷(解析版) 题型:选择题
下列方程式书写正确的是
A.苏打溶液中加入过量石灰水:HCO3-+Ca2++OH-=CaCO3↓+H2O
B.用硫酸酸化的橙色的重铬酸钾(K2Cr2O7)溶液与乙醇作用生成乙酸和草绿色三价铬,可以用于检测是否酒后驾驶:2Cr2O72-+3C2H5OH+16H+→4Cr3++3CH3COOH +11H2O
C.用铜为电极电解饱和食盐水:2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
D.表示乙醇燃烧热的热化学方程式(△H的绝对值正确):
C2H5OH(l)+3O2(g) 2CO2(g)+3H2O(g) △H= -1367.0kJ·mol-1
2CO2(g)+3H2O(g) △H= -1367.0kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
选项 | 实验操作 | 现象 | 结论 |
A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
B | 分别加热Na2CO3和NaHCO3固体 | 试管内壁都有水珠 | 两种物质均受热分解 |
C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 铝不能熔化 | 金属铝的熔点较高 |
D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,震荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二上第一阶段测化学试卷(解析版) 题型:选择题
将0.1 mol·L-1的氨水加水稀释至0.01 mol·L-1,稀释过程中温度不变,下列叙述正确的是
A.稀释后溶液中所有离子的浓度均减小
B.稀释后溶液中c(OH-)小于稀释前的1/10
C.稀释过程中氨水的电离平衡向左移动
D.稀释过程中溶液中 增大
增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com