
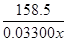 =
=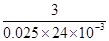 ,解得x=96.1%。
,解得x=96.1%。

科目:高中化学 来源:不详 题型:单选题
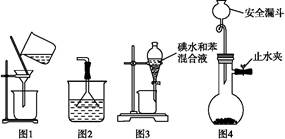
| A.用图1所示装置进行过滤,过滤时不断搅拌 |
| B.用图2所示装置吸收NH3制氨水 |
| C.用图3所示装置用苯萃取碘水中的碘,并把碘的苯溶液从漏斗下口放出 |
| D.用图4所示装置用石灰石与稀盐酸制取CO2气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用pH试纸鉴别 |
| B.分别用闻气味和pH试纸鉴别 |
| C.分别用BaCl2和NaOH溶液鉴别 |
| D.用Ba(OH)2溶液鉴别 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溴苯中混有溴,加入碳酸钠溶液,振荡,然后分液 |
| B.乙烷中混有乙烯,通入氢气,在一定条件下反应,使乙烯转化为乙烷 |
| C.硝基苯中混有浓HNO3和浓H2SO4,将其倒入NaOH溶液中,静置,分液 |
| D.乙烯中混有SO2和CO2,将其通入NaOH溶液中洗气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| A.H2O | B.CCl4 |
| C.NaHSO3 | D.HNO3 |
| T/℃ | 4 | 18 | 75 |
| 溶解度/g | 0.18 | 0.27 | 2.20 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
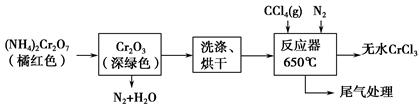
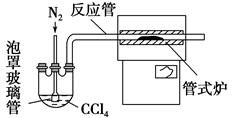
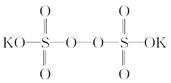 )具有强氧化性(常被还原为硫酸钾),80 ℃以上易发生分解。实验室模拟工业合成过硫酸钾的流程如下:
)具有强氧化性(常被还原为硫酸钾),80 ℃以上易发生分解。实验室模拟工业合成过硫酸钾的流程如下: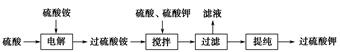
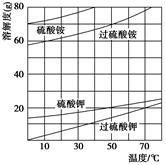
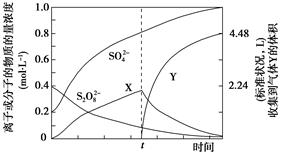
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
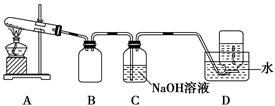
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硝酸,振荡 | 黑色固体溶解,并有气体产生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

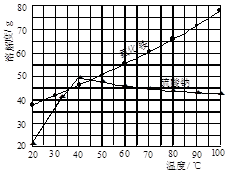
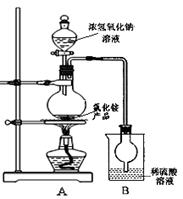
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分液、蒸馏 | B.蒸馏、分液 | C.分液、萃取 | D.萃取、分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com