
����Ŀ��ij��ѧ��ȤС�����Ժ���������������������������ͭ��Һ�����ۺ�ʵ�飺
��1����ȥFe2+��Fe3+���Ʊ�CuSO45H2O��������������̻ش����⣺
�й��������↑ʼ�����ͳ�����ȫ��pH���±���
�������� | Fe��OH��3 | Fe��OH��2 | Cu��OH��2 |
��ʼ������pH | 1.9 | 6.5 | 4.7 |
������ȫ��pH | 3.7 | 9.7 | 6.7 |
���Լ�X�Ļ�ѧʽΪ �� �����Լ�Y������ҺpH�ķ�Χ����
�ڲ���a�õ��IJ�������Ϊ�ձ�����������������b������Ϊ��
��2����֪��5Fe2++MnO4��+8H+=5Fe3++Mn2++4H2O�����ⶨ�����Һ�е�Fe2+��Ũ�ȣ�ȡ����Һ20.00mL����Ũ��Ϊ0.01molL��1������KMnO4��Һ�ζ������еζ���ʽ�У����������������ĸ��ţ��гֲ�������ȥ��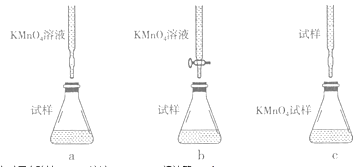
�ﵽ�յ�ʱ��ȥ����KMnO4��Һ12.00mL�������c��Fe2+��= ��
���𰸡�
��1��H2O2��3.7��4.7��©��������Ũ������ȴ�ᾧ
��2��b��0.03mol/L
���������⣺FeSO4��Fe2��SO4��3��CuSO4�Ļ����Һ�У����ݱ�������֪�������Լ�X����Fe2+����ΪFe3+ �� Ȼ�����CuO������Һ��pH��������ת��Ϊ�������õ���ҺA��Ȼ����ù��˷����õ�����Fe��OH��3����ҺB����ҺB�к���CuSO4 �� ����Һ����Ũ������ȴ�ᾧ�õ�CuSO4.5H2O
��1.�����Լ�X���������������Ҳ��������µ����ʣ�����X�Ļ�ѧʽΪH2O2 �� �����Լ�Y������ҺpH��ʹ��������ȫ������ͭ���Ӳ��ܳ���������pH�ķ�Χ��3.7��4.7�����Դ��ǣ�H2O2���ڲ���a�õ��IJ�������Ϊ�ձ�����������©��������b������Ϊ����Ũ������ȴ�ᾧ�����Դ��ǣ�©��������Ũ������ȴ�ᾧ��
��2.�����������Һ�����ԣ�Ӧ������ʽ�ζ���ʢ�ţ���ѡb��
����������Ũ��Ϊcmol/L��
5Fe2+ + MnO4�� +8H+ = 5Fe3+ + Mn2+ + 4H2O
5mol 1mol
0.02cmol 0.01mol/L��0.012L
5mol��1mol��0.02cmol����0.01mol/L��0.012L��
c=0.03��
���Դ��ǣ�b��0.03mol/L��


 ��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д�
��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д� Сѧ��ĩ���Ծ�ϵ�д�
Сѧ��ĩ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ͬ��������һ��ʢNO����һ��ʢN2��O2����ͬ��ͬѹ�£��������ڵ�����һ��������ͬ�ģ� ��
A. ԭ������ B. �������� C. �ܶ� D. ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ�����ᡢ���֪ʶ��ѧϰ�������Ѿ�֪�������������ƿ�����ΪijЩ����ĸ���������г�ʪ�����岻���ù����������Ƹ���� ( )
A.H2B.CO2C.COD.O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��CH3CH2CH2CH3(g)��6.5O2(g)![]() 4CO2(g)��5H2O(l)����H����2878kJ��mol��1 (CH3)2CHCH3(g)��6.5O2(g)�� 4CO2(g)��5H2O(l)����H����2869kJ��mol��1
4CO2(g)��5H2O(l)����H����2878kJ��mol��1 (CH3)2CHCH3(g)��6.5O2(g)�� 4CO2(g)��5H2O(l)����H����2869kJ��mol��1
����˵����ȷ����(����)
A����������Ӵ�������������춡�����
B����������ȶ��Դ����춡��
C���춡��ת��Ϊ������Ĺ�����һ�����ȹ���
D���춡������е�̼�����������Ķ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijǿ������ҺX������Fe3+��Fe2+��Ba2+��Al3+��NH4+��CO32����SiO32����SO42����NO3���е�һ�ֻ������ӣ�ȡ��Һ��������ʵ�飬��ʵ������ת����
����������Ϣ���ش��������⣺
��1��д���������������A�����ӷ���ʽ ��
��2������F�ĵ���ʽΪ �� ʵ���У����Թ۲쵽��Ӧ�ڵ������ǣ� ��
��3��������ҺI�д��ڵ������ӵķ����� ��
��4������G�Ļ�ѧʽΪ��д����Ӧ�ߵĻ�ѧ����ʽ ��
��5����ҺX�п϶������ڵ����������Բ���ȷ���Ƿ���ڵ����ӣ�������ȡX��Һ���Թ��У�ѡ�������Լ��е�һ�ּ���X��Һ�У���������Ϳ��жϣ�����Լ��� �� ��ѡ����ţ���pH��ֽ���ڷ�̪�Լ�����ʯ���Լ�����KSCN��Һ����NaOH��Һ����KMnO4��Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڻ�̬�����ԭ���У����ں����������������������ǣ� ��
A.����ʧȥ�ĵ����������
B.��������С�ĵ����������
C.p�����������һ������s�����������
D.���������������˶��ĵ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������䡱��������ָ��Ȼ������Ҫ�ɷ��Ǽ��飮��ҵ����̼��ˮ�ڸ����·�Ӧ�Ƶ�ˮú����ˮú������Ҫ�ɷ���CO��H2 �� ���������ԼΪ1��1.1mol CO������ȫȼ������CO2����ų�283kJ������1molH2��ȫȼ��������̬ˮ�ų�242kJ������1molCH4������ȫȼ������CO2�������̬ˮ�ų�802kJ������
��1��д��H2��ȫȼ��������̬ˮ���Ȼ�ѧ��Ӧ����ʽ����
��2������ˮú���������ɷ֣���ͬ״������������ȵ�������������ˮú������Ǽ������������ˮú���ų�CO2������Ǽ���ų�CO2�����������
��3������Ȼ������ˮú��������ȼ�ϣ�ͻ�����ŵ����� �� ����д2�㣩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״�ټ��غ�Ѫ�쵰���к��е���ҪԪ��������
A.I��FeB.Cu��MgC.I��MgD.Fe��Mg
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com