
【题目】关于水溶液中的离子平衡,下列说法正确的是
A.往![]() 稀溶液中加入NaOH固体,溶液中
稀溶液中加入NaOH固体,溶液中 变大
变大
B.等物质的量浓度的![]() 、
、![]() 、
、![]() 三种溶液中,
三种溶液中,![]() 的大小顺序为:
的大小顺序为:![]()
C.常温下![]() 的
的![]() 溶液和
溶液和![]() 的NaOH溶液等体积混合,溶液中离子浓度大小顺序为:
的NaOH溶液等体积混合,溶液中离子浓度大小顺序为:![]()
D.![]() 的
的![]() 溶液中:
溶液中:![]()
【答案】C
【解析】
A.加入NaOH固体,会导致钠离子浓度增大,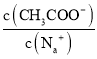 会变小,A错误;
会变小,A错误;
B.物质的量浓度相等的![]() 、
、![]() 、
、![]() 三种溶液中,
三种溶液中,![]() 中
中![]() 促进了
促进了![]() 的水解,
的水解,![]() 中铝离子水解抑制了铵根离子的水解,则
中铝离子水解抑制了铵根离子的水解,则![]() 中NH4+浓度大于
中NH4+浓度大于![]() ,所以
,所以![]() 由大到小的顺序为:
由大到小的顺序为:![]() ,B错误;
,B错误;
C.醋酸是弱酸,在溶液中存在电离平衡,所以在常温下pH=2 CH3COOH溶液中c(CH3COOH)>0.01mol/L,pH=2 的CH3COOH和![]() 的NaOH溶液等体积混合,CH3COOH过量,溶液为CH3COOH和CH3COONa的混合溶液,CH3COOH电离作用大于CH3COO-的水解作用,溶液显酸性,所以溶液中离子浓度大小顺序为:
的NaOH溶液等体积混合,CH3COOH过量,溶液为CH3COOH和CH3COONa的混合溶液,CH3COOH电离作用大于CH3COO-的水解作用,溶液显酸性,所以溶液中离子浓度大小顺序为:![]() ,C正确;
,C正确;
D.![]() 的
的![]() 溶液中,根据物料守恒,
溶液中,根据物料守恒,![]() ,D错误;
,D错误;
故合理选项是C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】由已知电离常数判断,下列关于SO2与Na2CO3(aq)反应的离子方程式的书写中,不合理的是( )
酸 | 电离常数 |
碳酸 | K1=4×10-7 K2=5.6×10-11 |
亚硫酸 | K1=1.54×10-2 K2=1.02×10-7 |
A.SO2+H2O+2CO32-=2HCO3-+SO32-
B.SO2+H2O+CO32-=H2O+CO2+SO32-
C.2SO2+2H2O+CO32-=H2O+CO2+2HSO3-
D.SO2+H2O+CO32-=HCO3-+HSO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是一种重要化工原料。
(1)德国化学家哈伯从1902年开始研究由氮气和氢气直接合成氨。
已知:①![]() △H=a kJ/mol
△H=a kJ/mol
②每破坏lmol有关化学键需要的能量如下表:
H-H | N-H | N≡N |
436kJ | 391kJ | 946k |
则a=_________________。
(2)下图为不同温度(T)、不同投料比[n(![]() )/n(
)/n(![]() )]时反应达到平衡时
)]时反应达到平衡时![]() 的转化率变化曲线。
的转化率变化曲线。
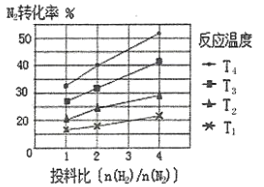
①![]() 、
、![]() 、
、![]() 、
、![]() 的大小关系为__________________。
的大小关系为__________________。
②保持温度和体积不变,提高投料比[n(![]() )/n(
)/n(![]() )],则重新达到平衡时,下列说法一定正确的是_______(填字母序号)。
)],则重新达到平衡时,下列说法一定正确的是_______(填字母序号)。
A.![]() 的浓度增大
的浓度增大
B.![]() 的转化率增大
的转化率增大
C.![]() 的体积分数增大
的体积分数增大
D.![]() 的浓度减小
的浓度减小
③温度为![]() 时,向2L密闭容器中加入1.0mol
时,向2L密闭容器中加入1.0mol![]() 和1.0mol
和1.0mol![]() ,若5min后反应达到平衡,则用v(
,若5min后反应达到平衡,则用v(![]() )表示该反应的平均速率为____________________;反应在
)表示该反应的平均速率为____________________;反应在![]() 时的平衡常数K=________________。
时的平衡常数K=________________。
(3)一种新型除烟气中氮氧化物的方法是采用![]() 作还原剂还原烟气中的氮氧化物且产物无污染,写出
作还原剂还原烟气中的氮氧化物且产物无污染,写出![]() 还原
还原![]() 的化学反应方程式_____________________________________。
的化学反应方程式_____________________________________。
(4)若用标准盐酸测定某稀氨水的浓度,应选择__________作指示剂;滴定过程中眼睛注视_____________。已知稀氨水体积为25.0mL,滴定结束测得消耗0.0100mol/L盐酸的平均体积为20.0mL,则该氨水的浓度为________________(保留2位有效数字);若滴定前滴定管尖嘴有气泡,滴定后尖嘴无气泡,则测定结果________(填“偏大”、“偏小”、“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在室温下,下列说法正确的是![]()
![]()
A.在滴有酚酞溶液的氨水里,加入![]() 至溶液恰好无色,则此时溶液的
至溶液恰好无色,则此时溶液的![]()
B.同![]() 的溶液:
的溶液:![]() 溶液,物质的量浓度最大的是
溶液,物质的量浓度最大的是![]()
C.有两种酸HA和HB,已知HA的酸性比HB弱,在物质的量浓度均为![]() 的NaA和NaB混合溶液中,有
的NaA和NaB混合溶液中,有![]()
D.pH相同的![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液、NaOH溶液,其浓度大小关系为:
溶液、NaOH溶液,其浓度大小关系为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系图中,A 是一种正盐,B 是气态氢化物,C 是单质,F 是强酸。当 X 无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当 X 是强碱时,过量的 B 跟 Cl2 反应除生成 C 外,另一产物是盐酸盐。
下列说法中不正确的是( )
![]()
A.当 X 是强酸时,A、B、C、D、E、F中均含同一种元素,F 可能是 H2SO4
B.当 X 是强碱时,A、B、C、D、E、F中均含同一种元素,F 是 HNO3
C.用 O2 代替 Cl2, 也能与 B 反应生成 C 物质
D.当 X 是强酸时,C 在常温下是一种易溶于酒精的固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A是一种重要的化工原料,其产量可以用来衡量一个国家的石油化工发展水平。A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型。根据如图回答下列问题:
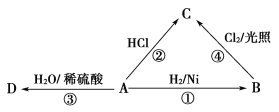
(1)写出A的电子式及空间构型:电子式___,空间构型___。
(2)②、④两种制备氯乙烷的方法中,方法___好。原因是__。
(3)写出③、④两步反应的化学方程式,并注明反应类型:
③___,反应类型___。
④__,反应类型__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,向 ![]() 二元弱酸
二元弱酸 ![]() 溶液中滴加
溶液中滴加 ![]() 溶液,溶液中的
溶液,溶液中的 ![]() ,
,![]() ,
, ![]() 的物质的量分数
的物质的量分数![]()
![]() 随 pH的变化如图所示。下列说法错误的是
随 pH的变化如图所示。下列说法错误的是![]()
![]()

![]() 已知
已知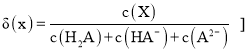
A.加入 ![]() 时,
时,![]()
B.当 ![]() ,
, ![]()
C.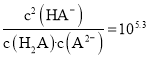
D.当混合溶液呈中性时,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别取浓度不同、体积均为20.00mL的3种HCl溶液,分别滴入浓度为1.000mol·L-1,0.1000mol·L-1和0.01000mol·L-1的NaOH溶液,测得3个反应体系的pH随V(NaOH)的变化的曲线如图,在V(NaOH)=20.00mL前后出现突跃。下列说法不正确的是

A. 3种HCl溶液的c(HCl):最大的是最小的100倍
B. 曲线a、b、c对应的c(NaOH):a>b>c
C. 当V(NaOH)=20.00mL时,3个体系中均满足:c(Na+)=c(Cl-)
D. 当V(NaOH)相同时,pH突跃最大的体系中的c(H+)最大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com