
【题目】用蒸馏水逐步稀释0.2 mol/L的稀氨水时,若温度不变,在稀释过程下列数据始终保持增大趋势的是( )
A.c(OH-)
B.c(NH4+)
C.c(NH3·H2O)
D.c(NH4+)/c(NH3·H2O)
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为TS(中文名![]() ,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
A. TS是第七周期第ⅦA族元素 B. TS的同位素原子具有相同的电子数
C. TS在同族元素中非金属性最弱 D. 中子数为176的TS核素符号是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是 ( )
A.原子晶体中一定不存在化学键B.离子晶体中只存在离子键
C.在共价化合物中一定有共价键D.非金属原子间只能形成共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个体积为1 L的密闭容器中发生某化学反应:2A(g) ![]() B(g)+C(g),三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800° C,实验Ⅲ在950°C。B、C的起始浓度都为0,反应物A的浓度(mol L-1)随时间(min)的变化如图所示。试回答下列问题:
B(g)+C(g),三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800° C,实验Ⅲ在950°C。B、C的起始浓度都为0,反应物A的浓度(mol L-1)随时间(min)的变化如图所示。试回答下列问题: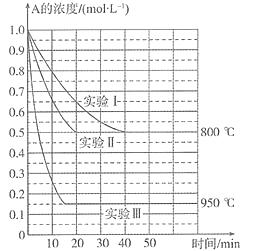
(1)在实验Ⅰ中,反应在2040 min内A的平均反应速率为mol L-1min-1。实验Ⅱ和实验Ⅰ相比,可能隐含的反应条件是。
(2)该反应的ΔH0,其判断理由是。
(3)实验Ⅰ第40 min末,若降低反应温度,达到新的平衡后,A的浓度不可能为________(填序号)。
A.0.35 mol·L1
B.0.4 mol·L1
C.0.7 mol·L1
D.0.8 mol·L1
(4)若反应在800°C进行,在该1 L的密闭容器中加入1 mol A、0.2 mol He,达到平衡时A的转化率应____________。
A.等于86%
B.等于50%
C.小于50%
D.在50%86%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列观点正确的是( )
A.H2O2中只存在极性键
B.在氧化钠中,只存在氧离子和钠离子的静电吸引作用
C.某化合物熔融态能导电,该化合物中一定有离子键
D.Na2O和Na2O2所含化学键类型完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示。该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。下列说法不正确的是
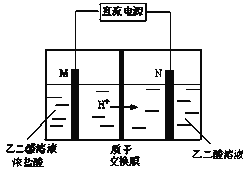
A.N电极上的电极反应式:HOOC-COOH+2e-+2H+=HOOC-CHO+H2O
B.若有2 mol H+ 通过质子交换膜并完全参与反应,则该装置中生成的乙醛酸为1 mol
C.M电极上的电极反应式为:2Cl--2e-=Cl2↑
D.乙二醛与M电极的产物反应生成乙醛酸的化学方程式: Cl2+OHC-CHO+ H2O = HOOC-CHO+2HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下:
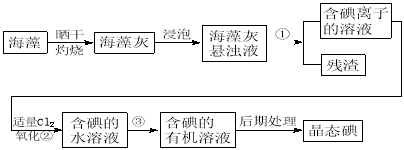
⑴ 在提取碘的过程中有关实验的操作名称:① ,③ ;写出过程②中有关反应的化学方程式: 。
⑵提取碘的过程中,可供选择的有机试剂是 。
A.酒精 B.苯 C.乙酸 D.四氯化碳
⑶为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器是 。
⑷从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏。指出如图所示实验装置中的错误之处: ; ; 。
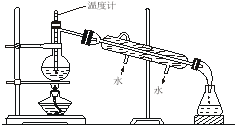
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,Zn、Cu与稀硫酸形成的原电池装置中,负极材料为___,负极反应式为____________________;正极材料为_____,正极反应式为____________________。
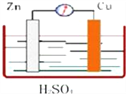
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锑(Sb)及其化合物的用途广泛。锑与砷同族,以辉锑矿为原料制备金属锑,其中一种工艺流程如图甲所示:
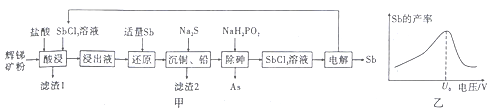
已知部分信息如下:
Ⅰ.辉锑矿(主要成分为Sb2S3,还含有As2S5、PbS、CuO和SiO2等);
Ⅱ.浸出液主要含盐酸和SbCl3,还含SbCl5、CuCl2、AsCl3和PbCl2等杂质;
Ⅲ.常温下,Ksp(CuS)=10×10-36、Ksp(PbS)=9.0×10-29
Ⅳ.H3PO2是一元中强酸。
回答下列问题:
(1)锑在周期表中的位置是___________,NaH2PO2的名称为________________。
(2)“酸浸”过程中SbCl5和Sb2S3反应有S生成,滤渣1的主要成分是__________(填化学式)。
(3)写出“还原”过程中反应的化学方程式:_____________________。
(4)已知浸出液中:c(Cu2+)=0.01mol·L-1、c(Pb2+)=0.10mol·L-1。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是________________(填化学式);加入硫化钠的量不宜过多,原因是__________________ 。
(5)在“除砷”过程中,氧化产物为H3PO4。该反应中还原剂、氧化剂的物质的量之比为______。
(6)“电解”中锑的产率与电压大小关系如图乙所示。当电压超过U0V时,锑的产率降低的原因可能是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com