
| A、84消毒液和洁厕灵混合使用会产生有毒气体:Cl-+ClO-+2H+=Cl2↑+H2O |
| B、向水玻璃中加入盐酸有白色沉淀生成:2H++SiO32-=H2SiO3↓ |
| C、SO2使紫色石蕊溶液变红色:SO2+H2O?2H++SO42- |
| D、漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3C1O-+3H2O=Fe(OH)3↓+3HClO |


科目:高中化学 来源: 题型:
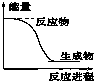
| A、碳与二氧化碳化合成为一氧化碳 |
| B、HCl分解为H2和Cl2 |
| C、Na与H2O反应 |
| D、Ba(OH)2?8H2O和NH4Cl晶体混合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某些馆的外壳使用非晶硅薄膜,以充分利用太阳能 |
| B、快餐盒用生物质材料“玉米塑料”(主要成分为可降解聚乳酸)做成 |
| C、使用的卫生纸都是再生纸 |
| D、把世博会期间产生的垃圾焚烧或深埋处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、甲醛的电子式: | ||||
B、用铜电极做盐酸溶液的电解实验:2H+2Cl
| ||||
C、溴乙烷与氢氧化钠水溶液共热:C2H5Br-+OH
| ||||
| D、澄清石灰水中加入过量的小苏打溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2L乙烯含有的极性共价键数为NA |
| B、常温下,5.6LNO和5.6LO2的混合气体中含有的分子数为0.5NA |
| C、16.9gBaO2固体中阴、阳离子总数为0.2NA. |
| D、常温常压下,28g氮气含有的核外电子数为10 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
| B、碳酸氢钠溶液与过量澄清石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| C、硫酸亚铁溶液中加入酸化的双氧水:Fe2++2H++H2O2=Fe3++2H2O |
| D、向明矾溶液中滴加过量氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3P2表示3P能级有两个轨道 |
| B、同一原子中1S、2S、3S电子的能量逐渐降低 |
| C、氢原子电子云的一个小黑点表示一个电子 |
| D、处于最低能量的原子叫基态原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
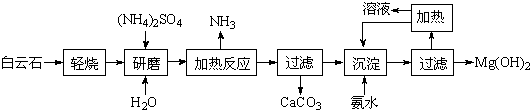
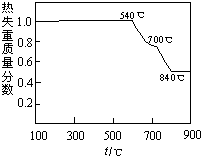
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验操作 | 实验现象或预期试验先行 | 现象解释(用离子方程式表示) | ||
| 猜想② | (1) | 溶液PH=8 | --- | |
| 向PH=2的硫酸中滴加Na2S2O3溶液 | (2) | S2O
| ||
| 猜想③ | 向新制氯水(PH<2)中滴加少许Na2S2O3溶液 | 氯水颜色变浅 | (3) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com