
 2C������������ 2 s���룩���� C ��Ũ��Ϊ 0.6 mol��L��1 ���������м���˵����������ȷ����
2C������������ 2 s���룩���� C ��Ũ��Ϊ 0.6 mol��L��1 ���������м���˵����������ȷ����| A�������� A ��ʾ�ķ�Ӧ��ƽ������Ϊ 0.3 mol��L��1��s��1 |
| B�������� B ��ʾ�ķ�Ӧ��ƽ������Ϊ 0.6 mol��L��1��s��1 |
| C��2 s ʱ���� A��ת����Ϊ70�� |
| D��2 s ʱ���� B��Ũ��Ϊ 0.7 mol��L��1 |
 ��ʦ�㲦��ϵ�д�
��ʦ�㲦��ϵ�д� Ӣ�żƻ���ĩ����ϵ�д�
Ӣ�żƻ���ĩ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2c(g)+D(g)�����ֲ�ͬ�����µķ�Ӧ���ʷֱ�Ϊ
2c(g)+D(g)�����ֲ�ͬ�����µķ�Ӧ���ʷֱ�Ϊ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
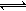 2SO2+ O2 ��H��0������SO3�ı仯����ͼʾ��
2SO2+ O2 ��H��0������SO3�ı仯����ͼʾ��
| A��a | B��b | C��c | D��d |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 NH3������ѹǿʹ���������Сʱ����ѧ��Ӧ���ʼӿ죬����Ҫԭ���ǣ� ��
NH3������ѹǿʹ���������Сʱ����ѧ��Ӧ���ʼӿ죬����Ҫԭ���ǣ� ��| A�������˶����ʼӿ죬ʹ��Ӧ����Ӽ����ײ�������� |
| B����Ӧ����ӵ��������ӣ�����Ӱٷ���������Ч��ײ�������� |
| C�����Ӽ�����С��ʹ���еĻ���Ӽ����ײ����Ϊ��Ч��ײ |
| D������Ӱٷ���δ�䣬����λ����ڻ���������ӣ���Ч��ײ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na2SO4��Һ | B��Na2CO3���� | C��NaNO3��Һ | D��CH3COONa���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| t | 200 | 400 | 800 |
| A | 1.45 | 1.28 | 1.00 |
| B | 0.38 | 0.72 | 1.28 |
| C | 0.095 | 0.18 | 0.32 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2 R(g)��2W(g)��4�ֲ�ͬ����µķ�Ӧ���ʷֱ����£����б�ʾ�÷�Ӧ���������ǣ� ��
2 R(g)��2W(g)��4�ֲ�ͬ����µķ�Ӧ���ʷֱ����£����б�ʾ�÷�Ӧ���������ǣ� �� | A��v(X) �� 0.15 mol��(L��S)��1 | B��v(Y) �� 0.60 mol��(L��S)��1 |
| C��v(R) �� 8.0 mol��(L��min)��1 | D��v(W) �� 0.45 mol��(L��S)��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2B��g����C��g��������ӦΪ���ȷ�Ӧ����ƽ��ʱ��Ҫʹ����Ӧ���ʽ��ͣ�A��Ũ������Ӧ��ȡ�Ĵ�ʩ�� �� ��
2B��g����C��g��������ӦΪ���ȷ�Ӧ����ƽ��ʱ��Ҫʹ����Ӧ���ʽ��ͣ�A��Ũ������Ӧ��ȡ�Ĵ�ʩ�� �� ��| A����ѹ | B��ʹ�ô��� |
| C����СC��Ũ�� | D������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����

 ��
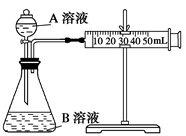
��
| ��� | A��Һ | B��Һ |
| �� | 2 mL 0.1 mol/L H2C2O4��Һ | 4 mL 0.01 mol/L KMnO4��Һ |
| �� | 2 mL 0.2 mol/L H2C2O4��Һ | 4 mL 0.01 mol/L KMnO4��Һ |
| �� | 2 mL 0.2 mol/L H2C2O4��Һ | 4 mL 0.01 mol/L KMnO4��Һ������MnSO4 |
 mol/L
mol/L H2C2O4��Һ����ȡ��֧�Թܸ�����4 mL 0.1 mol/L KMnO4��Һ������֧�Թֳܷ����飨����һ֧ʢ��H2C2O4��Һ��KMnO4��Һ���Թܣ���һ�������ˮ�У���һ�������ˮ�У�����һ��ʱ��ֱ���
H2C2O4��Һ����ȡ��֧�Թܸ�����4 mL 0.1 mol/L KMnO4��Һ������֧�Թֳܷ����飨����һ֧ʢ��H2C2O4��Һ��KMnO4��Һ���Թܣ���һ�������ˮ�У���һ�������ˮ�У�����һ��ʱ��ֱ��� ������¼��Һ��ɫ����ʱ�䡣��ʵ��Ŀ�����о� �Ի�ѧ��Ӧ���ʵ�Ӱ�죬������ͬѧʼ��û�п�����Һ��ɫ����ԭ���� ��
������¼��Һ��ɫ����ʱ�䡣��ʵ��Ŀ�����о� �Ի�ѧ��Ӧ���ʵ�Ӱ�죬������ͬѧʼ��û�п�����Һ��ɫ����ԭ���� ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com