
| A. | CaO | B. | Cl2 | C. | H2SO4 | D. | SO2 |
科目:高中化学 来源: 题型:实验题
 现有一瓶标签受到腐蚀(如图所示)的无色溶液,已知该溶液可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠、硫化钠中的一种,为确定溶液的成分,同学们进行了如下探究:
现有一瓶标签受到腐蚀(如图所示)的无色溶液,已知该溶液可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠、硫化钠中的一种,为确定溶液的成分,同学们进行了如下探究:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
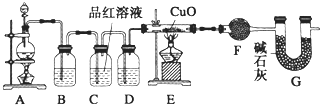
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
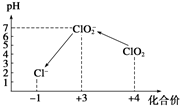
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验内容 | 试剂 | 实验现象 |
| 验证氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
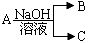 ,(若产物中有水生成则省略未表示出来).
,(若产物中有水生成则省略未表示出来).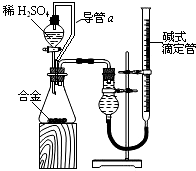
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 240 | 250 | 260 | 270 |
| 平衡总压强/kp | 5.7 | 8.3 | 12.0 | 17.1 |
| 平衡总浓度/mol•L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com