
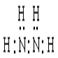 (2)AlO2-+2H2O
(2)AlO2-+2H2O Al(OH)3+OH-
Al(OH)3+OH-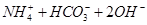



科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
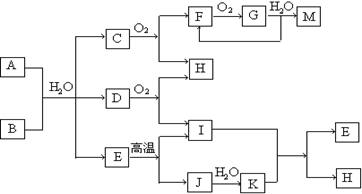
 G进行加压操作,产生的现象是 。
G进行加压操作,产生的现象是 。 溶液,并加热 。
溶液,并加热 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.质子数和中子数 |
| B.中子数和电子数 |
| C.核电荷数和核外电子层排布的电子数 |
| D.质量数和核外电子层排布的电子数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X的氢化物比R的氢化物稳定 |
| B.元素最高价氧化物水化物的酸性大小顺序是X >Y> Z |
| C.Y、R形成的化合物YR2能使KMnO4溶液褪色 |
| D.X、Z可形成化合物XZ5,分子中各原子均满足最外层8电子结构 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸雨样品露天放置一段时间,酸性增强,是由于雨水所含成分被氧化的原因 |
| B.N、P、As的非金属性逐渐增强 |
| C.因为氧化性HClO>稀H2SO4,所以非金属性Cl>S |
| D.钠原子在反应中失去的电子比铝原子少,故钠的金属性应弱于铝 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若XY3分子中X原子处于正三角形的中心,则XY3分子为非极性分子 |
| B.C2H5OH与C2H5Br相比,前者的沸点远高于后者,其原因是前者的分子间存在氢键 |
| C.同周期ⅠA族元素和 ⅦA族元素之间只能形成离子化合物 |
| D.由两种非金属元素组成的化合物分子中只可能有极性键,不会有非极性键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
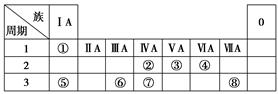
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.玻尔 | B.道尔顿 | C.汤姆生 | D.卢瑟福 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com