
W、X、Y、Z是原子序数依次增大的短周期元素。m、n、p是由这些元素组成的二元化合物,r是元素Y的常见单质,能使带火星的木条复燃,q的水溶液呈碱性,0.0l mol.L-l s溶液的pH为12,q、s的焰色反应均呈黄色。上述物质的转化关系如图所示。下列说法正确的是( )
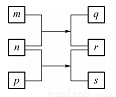
A.原子半径:W<X<Y<Z
B.通常状况下,X的氢化物可能呈气态、液态或固态
C.Y的氢化物的沸点比Z的氢化物的沸点高
D.由W、X、Y、Z四种元素只能组成一种化合物
科目:高中化学 来源:2016-2017学年福建省高一上期中化学卷(解析版) 题型:选择题
在一定条件下,可发生反应:XO3n-+Cl2 +2OH-=XO42-+2Cl-+H2O。则XO3 n-中X元素的化合价是
A.+4 B.+5 C.+6  D.+7
D.+7
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上阶段考二化学卷(解析版) 题型:选择题
在两个恒容的密闭容器中进行下列两个可逆反应:
甲:C(s)+H2O(g) CO(g)+H2(g);
CO(g)+H2(g);
乙:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
现有下列状态:
①混合气体平均相对分子质量不再改变
②恒温时,气体压强不再改变
③各气体组分浓度相等
④反应体系中温度保持不变
⑤断裂氢氧键速率是断裂氢氢键速率的2倍
⑥混合气体密度不变
⑦单位时间内,消耗水蒸气质量与生成氢气质量比为9∶1
其中能表明甲、乙容器中反应都达到平衡状态的是 ( )
A.①②⑤ B.③④⑤ C.⑥⑦ D.④⑤
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上学期期中质量检测化学试卷(解析版) 题型:选择题
化学与生产、生活密切相关。下列说法正确的是( )
A.人造纤维、合成橡胶和光导纤维都属于有机高分子化合物
B.大力实施矿物燃料“脱硫、脱硝技术”,减少硫的氧化物和氮的氧化物污染
C.用聚氯乙烯代替木材,生产包装盒、快餐盒等,以减少木材的使用
D.氢氧燃料电池、硅太阳能电池中都利用了原电池原理
查看答案和解析>>
科目:高中化学 来源:2017届河南省豫北推荐高三上学期精英对抗赛化学试卷(解析版) 题型:推断题
[化学——选修5:有机化学基础]酮洛芬是一种良好的非甾体抗炎镇痛药。下面是酮洛芬的中间体F的合成路线:
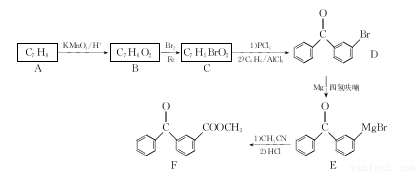
回答下列问题:
(1)A的结构简式为 ,F中含氧官能团名称为 。
(2)由A生成B的反应类型为 。
(3)由B生成C的化学方程式为 ,其反应类型为 。
(4)四氢呋喃是一种性能优良的溶剂,可由呋喃加氢得到。呋喃的结构简式为 ,则四氢呋喃的结构简式为 。
,则四氢呋喃的结构简式为 。
(5)W是C的同分异构体,W既能发生银镜反应,又能与FeCl3溶液发生显色反应,W的结构共有 种(不含立体结构);写出-种符合下列条件的F的同分异构体的结构简式: 。
①能与FeCl3发生为色反应
②核磁共振氢谱有6个吸收峰
(6)参照上述合成路线,以苯和CH3CN为起始原料,设计制备的 合成路线:
合成路线:
查看答案和解析>>
科目:高中化学 来源:2017届河南省豫北推荐高三上学期精英对抗赛化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数值。下列叙述正确的是( )
A.标准状况下,22.4 L乙烷中所含共价键数目为6NA
B.100 mL0.1 mol.L-1 FeCl3溶液中含有Fe3+的数目为0.01NA
C.0.2 mol Zn与一定量浓硫酸恰好完全反应,生成的气体分子数为0.2NA
D.1 L0.1 mol.L-l NaHCO3溶液中HC03-和CO32-离子数之和为0.1NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高一上月考三化学卷(解析版) 题型:选择题
将一定量的Na、Na2O、Na2O2的混合物与足量的水反应,在标准状况下得到a L混合气体。将该混合气体通过电火花引燃,恰好完全反应,则原混合物中Na、Na2O、Na2O2的物质的量之比可能为( )
A.2:1:2 B.1:1:2 C.2:2:1 D.1:1:1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高一上期中化学卷(解析版) 题型:填空题
在2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O反应中:
(1)氧化剂是(填化学式) ,还原剂是(填化学式) 。
(2)在该反应中,若消耗了15.8g KMnO4,则转移了 mol 电子。
(3)用双线桥表示高锰酸钾和浓盐酸反应的电子转移方向和数目。
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上期中化学试卷(解析版) 题型:填空题
在一容积为2 L的密闭容器内为加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g) ΔH<0反应中NH3的物质的量浓度的变化的情况如图所示:
2NH3(g) ΔH<0反应中NH3的物质的量浓度的变化的情况如图所示:
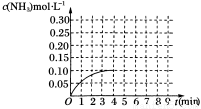
(1)根据上图,计算从反应开始到平衡时,平均反应速率υ(NH3)=___________ mol·L-1·min-1。
(2)反应达到平衡后,第5分钟末,保持其他条件不变,若改变反应温度,则NH3的物质的量浓度不可能为____________(填字母序号)。
A.0.20 mol·L-1 B.0.12 mol·L-1
C.0.10 mol·L-1 D.0.08 mol·L-1
(3)该反应平衡常数K=____________。
(4)反应达到平衡后,第5分钟末,保持其他条件不变,若只把容器的体积缩小一半,平衡________移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数____________(填“增大”、“减小”或“不变”)。
(5)在第5分钟 末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(设此时NH3的浓度为0.25 mol·L-1)。请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。
末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(设此时NH3的浓度为0.25 mol·L-1)。请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com