
X、Y、Z三种元素的原子,其最外层电子排布分别为ns1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是( )
A.XYZ2 B.X2YZ3
C.X2YZ2 D.XYZ3
科目:高中化学 来源: 题型:
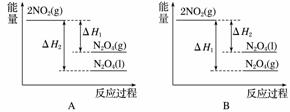
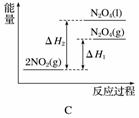
]已知:2NO2(g)??N2O4(g) ΔH1
2NO2(g)??N2O4(l) ΔH2
下列能量变化示意图中,正确的是(选填字母)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图表示水中c(H+)和c(OH-)的关系,下列判断错误的是 ( )
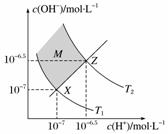
A.两条曲线间任意点均有c(H+)×c(OH-)=Kw
B.M区域内任意点均有c(H+)<c(OH-)
C.图中T1<T2
D.XZ线上任意点均有pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学兴趣小组的同学对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定。请回答下列问题:
(1)甲同学运用沉淀法测定样品中NaOH的含量。该同学选用的药品除样品外,还应有________;实验中应测定的数据有________。
(2)乙同学运用滴定法测定样品中NaOH的含量。
①用分析天平准确称取该样品5.000 0 g,全部溶于水配制成1 000.0 mL溶液。用碱式滴定管量取20.00 mL所配溶液放在锥形瓶中,滴加几滴指示剂,待测。滴定管在使用前除洗涤外,还应____________________________________。
②用浓度为0.100 0 mol·L-1的盐酸标准溶液进行滴定。开始滴定前的一步操作是________。
③滴定过程中用pH计测定锥形瓶中溶液的pH,临近滴定终点时测定pH应每滴一滴测一次。
④滴定过程中,锥形瓶中溶液的pH变化如下:
| V(HCl)/mL | 0.00 | 12.00 | 18.00 | 22.00 | 23.00 | 23.96 | 24.00 | 24.04 | 25.00 | 26.00 | 30.00 |
| pH | 13.1 | 12.6 | 12.2 | 11.7 | 11.4 | 9.9 | 7.0 | 4.0 | 2.7 | 2.4 | 1.9 |
请在坐标图中绘制出上述中和滴定的曲线。

⑤如表所示是几种酸碱指示剂的变色范围,根据你所作的中和滴定曲线分析,上述中和滴定中应选用的指示剂是________。
| 指示剂 | 变色范围(pH) | 颜色 | |
| 酸 | 碱 | ||
| 甲基橙 | 3.1~4.4 | 红 | 黄 |
| 石蕊 | 5.0~8.0 | 红 | 蓝 |
| 酚酞 | 8.2~10.0 | 无 | 红 |
⑥样品中,NaOH的质量百分含量为____________。
答案 (1)MgCl2溶液 样品质量和加入足量MgCl2溶液后生成的沉淀质量
(2)①检漏、润洗 ②调节盛标准液的滴定管的液面于“0”刻度或“0”刻度以下
④滴定曲线如图所示
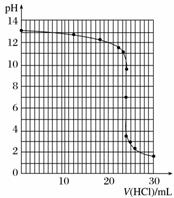
⑤甲基橙或酚酞 ⑥96%
查看答案和解析>>
科目:高中化学 来源: 题型:
根据信息回答下列问题:
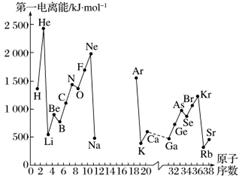
A.第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的最低能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
B.不同元素的原子在分子内吸引电子的能力大小可用数值表示,该数值称为电负性。一般认为:如果两个成键原子间的电负性差值大于1.7,原子之间通常形成离子键;如果两个成键原子间的电负性差值小于1.7,通常形成共价键。下表是某些元素的电负性值:
| 元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| 电负性值 | 1.0 | 1.5 | 2.0 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 |
(1)认真分析信息A图中同周期元素第一电离能的变化规律,推断第三周期Na~Ar这几种元素中,Al的第一电离能的大小范围为______<Al<______(填元素符号)。
(2)从信息A图中分析可知,同一主族元素原子的第一电离能I1的变化规律是________________。
(3)信息A图中第一电离能最小的元素在周期表中的位置是________周期________族。
(4)根据对角线规则,Be、Al元素最高价氧化物对应水化物的性质相似,它们都具有________性,其中Be(OH)2显示这种性质的离子方程式是________________________________________________________________________。
(5)通过分析电负性值的变化规律,确定Mg元素的电负性值的最小范围________________。
(6)请归纳元素的电负性和金属性、非金属性的关系是________________。
(7)从电负性角度,判断AlCl3是离子化合物还是共价化合物,说出理由并写出判断的方法________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
基态Fe原子有________个未成对电子。Fe3+的电子排布式为________。可用硫氰化钾检验Fe3+,形成的配合物的颜色为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A.除0族元素外,短周期元素的最高化合价在数值上都等于该元素所属族的族序数
B.除短周期外,其他周期均为18种元素
C.副族元素没有非金属元素
D.碱金属元素是指ⅠA族(除H外)的所有的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
正误判断,正确的划“√”,错误的划“×”
(1)(2014·高考试题组合)
①施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用,是因为K2CO3与NH4Cl反应生成氨气会降低肥效( )
(2014·新课标全国卷Ⅰ,8C)
②小苏打是面包发酵粉的主要成分之一( )
(2014·福建理综,6D)
③将NH4Cl溶液蒸干制备NH4Cl固体( )
(2014·福建理综,8B)
④NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中( )
(2014·天津理综,3B)
(2)(2013·高考试题组合)
①向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成( )
(2013·重庆理综,2C)
②饱和小苏打溶液中:c(Na+)=c(HCO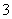 )( )
)( )
(2013·广东理综,12B)
③室温下,对于0.1 mol·L-1氨水,用HNO3溶液完全中和后,溶液不显中性( )
(2013·福建理综,8C)
④已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO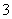 +H2O??H2SO3+OH-①
+H2O??H2SO3+OH-①
HSO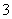 ??H++SO
??H++SO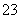 ②
②
向0.1 mol·L-1的NaHSO3溶液中
a.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO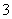 )增大( )
)增大( )
(2013·安徽理综,13A)
b.加入少量NaOH溶液,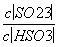 、
、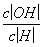 的值均增大( )
的值均增大( )
(2013·安徽理综,13C)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com