
【题目】下列实验能达到目的的是( )
选项 | 目的 | 实验 |
A | 检验某品牌食盐是否为加碘盐 | 将样品溶解后滴加淀粉溶液 |
B | 检验补铁剂硫酸亚铁片是否部分氧化 | 取样品溶解于水,滴加铁氰化钾溶液 |
C | 鉴别葡萄糖溶液和蔗糖溶液 | 分别取样,滴加银氨溶液,水浴加热 |
D | 证明 | 将 |
A. AB. BC. CD. D
科目:高中化学 来源: 题型:
【题目】某Na2CO3、NaAlO2的混合溶液中逐滴加入1molL1的盐酸,测得溶液中的CO32、HCO3、AlO2、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。则下列说法正确的是( )(已知:H2CO3的电离平衡常数K1 = 4.3×107,K2 = 5.6×1011;Al(OH)3的酸式电离平衡常数K=6.3×1013)

A. a曲线表示的离子方程式为:AlO2+4H+ = Al3+ + 2H2O
B. M点时生成的CO2为0.05 mol
C. 原混合溶液中的CO32与AlO2的物质的量之比为1:2
D. V1:V2=1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由4个碳原子结合成的6种有机物(氢原子没有画出)
![]()
(1) 写出有机物(a)的系统命名法的名称___________________。
(2) 有机物(a)有一种同分异构体,试写出其结构简式__________________。
(3) 上述有机物中与(c)互为同分异构体的是________(填代号)。
(4) 任写一种与(e)互为同系物的有机物的结构简式____________。
(5) 上述有机物中不能与溴反应并使其褪色的有________(填代号)。
(6) (a)(b)(c)(d)四种物质中,4个碳原子一定处于同一平面的有________(填代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将CO2气体缓缓地通入到含KOH、Ba(OH)2和K[Al(OH)4]的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示。下列关于整个反应进程中的各种描述不正确的是
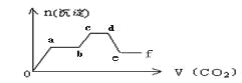
A. o—a段反应的化学方程式是:Ba(OH)2 + CO2 = BaCO3↓+ H2O
B. b—c段反应的离子方程式是:2[Al(OH)4]-+ CO2 = 2Al(OH)3↓ +CO32-+ H2O
C. a—b段与c—d段所发生的反应相同
D. d—e段沉淀的减少是由于碳酸钡固体的消失所致
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于“摩尔”的理解正确的是( )
A. 1摩尔H2O质量为18g
B. 摩尔是国际科学界建议采用的一种物理量,简称摩,符号为 mol
C. 22.4LO 2 中所含氧气分子为1 摩尔
D. 1mol 氧含 6.02×10 23 个O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(![]() )常温下为无色液体,熔点-54.1℃,沸点69.l℃,100℃以上或长时间存放易分解,在潮湿空气中“发烟”。可用作有机化学的氯化剂,在药物和染料的制取中也有重要作用。实验室中可用干燥的氯气和二氧化硫在活性炭催化下制取硫酰氯:
)常温下为无色液体,熔点-54.1℃,沸点69.l℃,100℃以上或长时间存放易分解,在潮湿空气中“发烟”。可用作有机化学的氯化剂,在药物和染料的制取中也有重要作用。实验室中可用干燥的氯气和二氧化硫在活性炭催化下制取硫酰氯:![]()
![]() ,实验装置如图所示(部分夹持装置未画出):
,实验装置如图所示(部分夹持装置未画出):
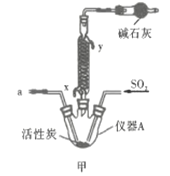
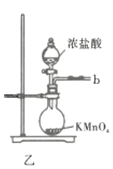
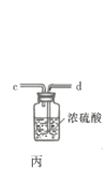
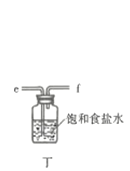
回答下列问题:
(1)仪器A的名称为___________;按氯气气流从左到右的方向,合理的装置接口连接顺序为___________。
(2)甲中蛇形冷凝管冷却水的入口是___________(填“x”或“y”),干燥管中盛装碱石灰的作用为___________。
(3)长期存放的硫酰氯会发黄,其原因可能为______________________。
(4)![]() 在潮湿空气中“发烟”,反应的化学方程式为______________________。
在潮湿空气中“发烟”,反应的化学方程式为______________________。
(5)工业上制得的硫酰氯常混有硫酸盐杂质,可用滴定法测定其纯度:称取1.500g样品,加入到盛有100mL 0.5000 mol![]() 溶液的烧杯中加热充分反应,冷却后转移至250mL___________中,经过___________、轻摇、定容、摇匀,配制得到待测溶液。取25.00mL待测溶液于锥形瓶中,滴加2滴甲基橙,用0.1000
溶液的烧杯中加热充分反应,冷却后转移至250mL___________中,经过___________、轻摇、定容、摇匀,配制得到待测溶液。取25.00mL待测溶液于锥形瓶中,滴加2滴甲基橙,用0.1000![]() 标准溶液滴定,到达滴定终点的现象为___________;重复滴定三次,平均消耗标准溶液10.00mL,测得该样品的纯度为___________。
标准溶液滴定,到达滴定终点的现象为___________;重复滴定三次,平均消耗标准溶液10.00mL,测得该样品的纯度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质的有机溶液迁移入 MnO2 晶格中,生成 LiMnO2。下列说法正确的是
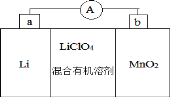
A. 外电路的电流方向是由 a 极流向 b 极。
B. 电池b 极反应式为 MnO2+e-+Li+=LiMnO2
C. 可用水代替电池中的混合有机溶剂
D. a 极发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 (1)一块表面已被氧化为Na2O的钠块10.8 g,将其投入100 mL水中,产生标准状况下2.24 L气体(假设溶液体积变化可忽略)。则这块钠块中所含单质钠的质量分数是_________(保留小数点后一位)。所得溶液中溶质的物质的量浓度为_________。
(2)已知实验室也可用KMnO4和浓盐酸反应制备氯气,化学方程式为2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O,请用双线桥法表示出电子转移的方向和数目______________。该反应中还原产物为______________。
(3)碳酸氢钠俗称小苏打,请写出碳酸氢钠的电离方程式_______________________。碳酸氢钠既能与酸反应又能与碱反应,请写出碳酸氢钠溶液与NaOH溶液反应的离子方程式
_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产纯碱的工艺流程示意图如下:

完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。
A__________________________________B__________________________________
(2)实验室提纯粗盐的实验操作依次为:
取样、______、沉淀、______、______、冷却结晶、______、烘干。
(3)工业生产纯碱工艺流程中,碳酸化时产生的现象是____________________________。
碳酸化时没有析出碳酸钠晶体,其原因是_______________________________________。
(4)碳酸化后过滤,滤液D最主要的成分是_____________________________(填写化学式),检验这一成分的阴离子的具体方法是:________________________________________。
(5)氨碱法流程中氨是循环使用的,为此,滤液D加入石灰水产生氨。加石灰水后所发生的反应的离子方程式为:_________________________________________________________
滤液D加石灰水前先要加热,原因是_____________________________________________。
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:
_____________________________________________________________________________
(注明你的表达式中所用的有关符号的含义)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com