
����Ŀ���£�N2H4����Ҫ�������������������ȼ�ϡ�
(1) ��֪ �� 2O2(g)��N2(g) === N2O4(l) ��H��a kJ��mol-1
�� N2(g)��2H2(g) === N2H4(l) ��H��b kJ��mol-1
�� 2H2(g) + O2(g) = 2H2O(g) ��H��c kJ��mol-1
ij�ͺŻ������Һ̬�º�Һ̬N2O4���ƽ�����ȼ��������������Ⱦ�����塣д����Ӧ���Ȼ�ѧ����ʽ____��ƫ�����£�1,1-�����£�Ҳ��һ�ָ���ȼ�ϣ�д����ṹ��ʽ______��
��2���¿��Գ�ȥˮ�е��ܽ��������������ܲ������ѭ����д���÷�Ӧ�Ļ�ѧ����ʽ________�������ϣ�ÿ����64 g�¿ɳ�ȥ��״����O2________L
��3����ѧ��������Ϊȼ�ϵ�ص�ȼ�ϣ���ؽṹ��ͼ1��ʾ��
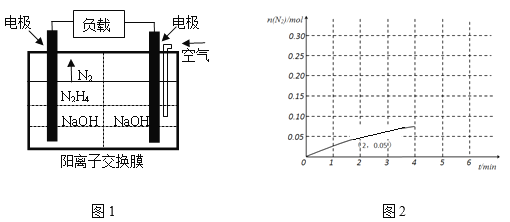
д����ظ����ĵ缫��Ӧʽ��________��
��4��N2H4���ض������£�303K��Pt��Ni�����������Է������ַֽ⣺N2H4(g) ![]() 2H2(g)��N2(g)����2 L���ܱ������м���0.1 mol N2H4(g)�����0-4������N2�����ʵ�����ʱ��ı仯������ͼ2��ʾ��д��0-2������H2��ƽ����Ӧ����v(H2)=________��
2H2(g)��N2(g)����2 L���ܱ������м���0.1 mol N2H4(g)�����0-4������N2�����ʵ�����ʱ��ı仯������ͼ2��ʾ��д��0-2������H2��ƽ����Ӧ����v(H2)=________��
���𰸡�2N2H4(l)��N2O4(l) ===3N2(g)��4H2O(g) ��H��(2c��a��2b) kJ��mol-1  N2H4��O2===2H2O��N2 44.8 N2H4��4OH-��4e-=== N2����4H2O 0.025 mol��L-1��min-1
N2H4��O2===2H2O��N2 44.8 N2H4��4OH-��4e-=== N2����4H2O 0.025 mol��L-1��min-1
��������
��1�����ø�˹�������Һ̬�º�Һ̬N2O4��ȼ��������������Ⱦ��������Ȼ�ѧ����ʽ������ƫ�����µ����֣�1,1-�����£���д�ṹ��ʽ��
��2���¿��Գ�ȥˮ�е��ܽ������������ܲ������ѭ���ĵ������ɴ�д���÷�Ӧ�Ļ�ѧ����ʽ��������ÿ����64 g�¿ɳ�ȥ��״����O2�����
��3������Ϊȼ�ϵ�ȼ�ϵ�أ�ȼ���²��뷴Ӧ�ĵ缫Ϊ��������ʧȥ���ӣ�
��4����ͼ���Կ�����0-2�����ڣ�![]() n(N2)=0.05mol,�ɴ���0-2�����ڵ�v(N2)����������֮�ȵ��ڻ�ѧ������֮�����v(H2)��
n(N2)=0.05mol,�ɴ���0-2�����ڵ�v(N2)����������֮�ȵ��ڻ�ѧ������֮�����v(H2)��
��1���� 2O2(g)��N2(g) === N2O4(l) ��H��a kJ��mol-1
�� N2(g)��2H2(g) === N2H4(l) ��H��b kJ��mol-1
�� 2H2(g) + O2(g) = 2H2O(g) ��H��c kJ��mol-1
���ݸ�˹����2![]() ��
��![]() 2
2![]() ��
��![]() �ٵã�2N2H4(l)��N2O4(l) ===3N2(g)��4H2O(g) ��H��(2c��a��2b) kJ��mol-1��1,1-�����µĽṹ��ʽΪ��
�ٵã�2N2H4(l)��N2O4(l) ===3N2(g)��4H2O(g) ��H��(2c��a��2b) kJ��mol-1��1,1-�����µĽṹ��ʽΪ��![]() ��
��
�������2N2H4(l)��N2O4(l) ===3N2(g)��4H2O(g) ��H��(2c��a��2b) kJ��mol-1��![]() ��
��
��2���������֪���º�������Ӧ�����ɵ�����ˮ���仯ѧ����ʽΪ��N2H4��O2===2H2O��N2��������64 g�¿ɳ�ȥ��״����O2���ΪVL��������������ʽ�ɵã�32:22.4=6.4��V�����V=44.8L��
�������N2H4��O2===2H2O��N2��44.8��
��3������Ϊȼ�ϵ�ȼ�ϵ�أ�ȼ���²��뷴Ӧ�ĵ缫Ϊ��������ʧȥ���ӣ��ڼ��������£��缫��ӦʽΪ��N2H4��4OH-��4e-=== N2����4H2O��
�������N2H4��4OH-��4e-=== N2����4H2O��
��4����ͼ���Կ�����0-2�����ڣ�![]() n(N2)=0.05mol��
n(N2)=0.05mol��![]() c(N2)=0.05mol/2L=0.025mol/L��v��N2��=
c(N2)=0.05mol/2L=0.025mol/L��v��N2��=![]() c/
c/![]() t=
t=![]() =0.0125mol��L-1��min-1����������֮�ȵ��ڻ�ѧ������֮�ȿɵã�v(H2)=2 v��N2��=0.025 mol��L-1��min-1��
=0.0125mol��L-1��min-1����������֮�ȵ��ڻ�ѧ������֮�ȿɵã�v(H2)=2 v��N2��=0.025 mol��L-1��min-1��
�������0.025 mol��L-1��min-1��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���� �� ��
A. ����AgCl��AgI���������Һ��c(Ag��)��c(C1��)��c(I��)
B. �ں���BaSO4��������Һ�м���Na2SO4���壬c(Ba2��)����
C. AgCl��ͬŨ�ȵ�CaCl2��NaCl��Һ�е��ܽ����ͬ
D. CaCO3 ������ϡ���ᣬ�������ڴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A. �����ܽ�ˮ���е�CaCO3�� CaCO3 + 2H+= Ca2++ H2O + CO2��
B. ���Ե缫��ⱥ��MgCl2��Һ�� Mg2++2Cl�� + 2H2O ![]() Mg(OH)2�� + H2�� + Cl2��
Mg(OH)2�� + H2�� + Cl2��
C. ��������Һ��ͨ��������CO2��![]() +H2O+CO2��
+H2O+CO2��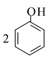 +
+![]()
D. ��������Һ������ȩ�е�ȩ����CH3CHO��![]() ��2OH��
��2OH��![]() CH3COONH4��H2O��2Ag����3NH3��
CH3COONH4��H2O��2Ag����3NH3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��������ӵ�ص��ܷ�ӦʽΪ2Li+FeS=Fe+Li2S��LiPF6��SO(CH3)2Ϊ����ʣ��øõ��Ϊ��Դ��⺬�����Է�ˮ���õ�����Ni��ʵ��װ����ͼ��ʾ������˵������ȷ����

A. �缫YΪLi
B. �������У�b��NaCl��Һ�����ʵ���Ũ�Ƚ����ϼ�С
C. X����ӦʽΪFeS+2Li++2e-=Fe+Li2S
D. ����ͼ��������Ĥȥ������a��b���Һϲ������ⷴӦ�ܷ���ʽ�����ı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ijЩ�������ȡ���ռ���β������װ����ͼ��ʾ��ʡ�Լгֺ;���װ�ã������ô�װ�úͱ����ṩ������������ʵ�飬�������ѡ����
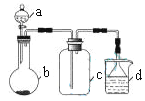
ѡ�� | a�е����� | b�е����� | c���ռ������� | d�е����� |
A | Ũ��ˮ | CaO | NH3 | H2O |
B | Ũ���� | Na2SO3 | SO2 | NaOH��Һ |
C | ϡ���� | Cu | NO2 | H2O |
D | Ũ���� | MnO2 | Cl2 | NaOH��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ȤС���ijƷ��������Ħ�����ɷּ��京����������̽����
������ϣ�������Ħ������̼��ơ�����������ɣ������������ɷ���������ʱ���������ɡ�
I.Ħ���������������Ķ��Լ���
ȡ����������Ʒ����ˮ��ֽ��衢���ˡ�
(1)�������м������NaOH��Һ�����ˡ�����������NaOH��Һ��Ӧ�����ӷ���ʽ��___��
(2)��(1)������Һ����ͨ�����������̼���ټ������ϡ���ᣬ�۲쵽��������_______��
��.������Ʒ��̼��ƵĶ����ⶨ
������ͼ��ʾװ��(ͼ�мг�������ȥ)����ʵ�飬��ַ�Ӧ�ⶨC�����ɵ�BaCO3������������ȷ��̼��Ƶ�����������

����ʵ����̻ش��������⣺
(3)����a��������_______��
(4)ʵ����������������ͨ������������ó��˿ɽ���B��C�еķ�Ӧ���⣬���У�____��
(5)C�з�Ӧ����BaCO3�Ļ�ѧ����ʽ��_____��
(6)���и����ʩ�У�������߲ⶨȷ�ȵ���____(����)��
a.�ڼ�������֮ǰ��Ӧ�ž�װ���ڵ�CO2���壻
b.�μ�����˹��죻
c.��A-B֮������ʢ��Ũ�����ϴ��װ�ã�
d.��B-C֮������ʢ�б���̼��������Һ��ϴ��װ�á�
(7)ʵ����ȷ��ȡ8.00g��Ʒ���ݣ��������βⶨ�����BaCO3��ƽ������Ϊ3.94g������Ʒ��̼��Ƶ���������Ϊ______(����3λ��Ч����)��
(8)������Ϊ���زⶨC�����ɵ�BaCO3������ֻҪ�ⶨװ��C����CO2ǰ��������һ������ȷ��̼��Ƶ���������������Ϊ���˷����ⶨ�Ƿ����_____(��������������)����������������_____(����ƫ��������ƫ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳɰ���Ӧ��N2+3H22NH3��һ�����ȵĿ��淴Ӧ����Ӧ�����Ǹ��¡���ѹ��������Ҫ���ʵĴ�������֪�γ�![]() ����
����![]() ����1molN��N�ų������ֱ�Ϊ436kJ��391kJ��946kJ����
����1molN��N�ų������ֱ�Ϊ436kJ��391kJ��946kJ����
(1)����ȫ��Ӧ����2mol![]() ��______
��______![]() ���������������ų���
���������������ų���![]() ����______kJ��
����______kJ��
(2)�����![]() ��
��![]() ��ϣ�ʹ���ַ�Ӧ���ų���������С��������ֵ����ԭ����______��
��ϣ�ʹ���ַ�Ӧ���ų���������С��������ֵ����ԭ����______��
(3)ʵ����ģ�ҵ�ϳɰ�ʱ�����ݻ�Ϊ2L���ܱ������ڣ���Ӧ����10min������![]() ������
������![]() ��ʾ�Ļ�ѧ��Ӧ����Ϊ______��
��ʾ�Ļ�ѧ��Ӧ����Ϊ______��
(4)���ĸ���ͬ�����У���ͬ�����½��кϳɰ���Ӧ����������ͬʱ���ڲⶨ�Ľ�����жϸ÷�Ӧ�������ɴ�С��˳����______![]() �ñ����д
�ñ����д![]() ��
��
A.v(NH3)=0.5mol/(Lmin) B. v(H2)=0.3mol/(Lmin)
C.v(N2)=0.2mol/(Lmin) D. v(H2)=0.01mol/(Lmin)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��Ӧ�IJ�����������ͬ���칹�����
��CH3CH2CH2Br�ڼ�����Һ��ˮ�⡡�ڼױ��ڴ�����������Cl2���������ϵ�ȡ����Ӧ����2���ȶ�����NaOH�Ҵ���Һ���ȷ�Ӧ �� �ڴ����Ĵ�����������ȫ�ӳ� �������ϩ��
�ڴ����Ĵ�����������ȫ�ӳ� �������ϩ�� ��������ʵ�����Br2�����ӳɷ�Ӧ
��������ʵ�����Br2�����ӳɷ�Ӧ
A. �٢ڢ� B. �٢ڢ� C. �ڢۢ� D. �ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������Ȼ�ѧ����ʽ���ش��������⣺
2H2(g)+O2(g)=2H2O��1�� ��H=571.6 kJ �� mol1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ��H=2 220 kJ �� mol1
��1��H2��ȼ����Ϊ_______��C3H8��ȼ����Ϊ_______��
��2��1 mol H2��2 mol C3H8��ɵĻ��������ȫȼ���ͷŵ�����Ϊ______________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com