
A.Ba(OH)2(aq)+2HCl(aq) ![]() BaCl2(aq)+2H2O(l)����H��+114.6 kJ��mol-1??
BaCl2(aq)+2H2O(l)����H��+114.6 kJ��mol-1??
B.Ba(OH)2(aq)+2HCl(aq) ![]() BaCl2(aq)+2H2O(l)����H����114.6 kJ��mol-1??
BaCl2(aq)+2H2O(l)����H����114.6 kJ��mol-1??
C.![]() Ba(OH)2(aq)+HCl(aq)
Ba(OH)2(aq)+HCl(aq) ![]()
![]() BaCl2(aq)+H2O(l)����H����57.3 kJ��mol-1??
BaCl2(aq)+H2O(l)����H����57.3 kJ��mol-1??
D.![]() Ba(OH)2(aq)+HCl(aq)
Ba(OH)2(aq)+HCl(aq) ![]()
![]() BaCl2(aq)+H2O(l)����H��+57.3 kJ��mol-1??
BaCl2(aq)+H2O(l)����H��+57.3 kJ��mol-1??
 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д� ѧҵ����һ��һ��ϵ�д�
ѧҵ����һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ���� ( )
A���ϳɰ����������н�NH3Һ�����룬�ɼӿ�����Ӧ���ʣ����N2��H2��ת����
B����1 mol Ba(OH)2��ϡ��Һ�ͺ�1 mol H2SO4��ϡ��Һ��Ӧ�ͷ�����akJ�����ʾ�÷�Ӧ�к��ȵ��Ȼ�ѧ��Ӧ����ʽΪ��OH��(aq)��H��(aq)=H2O(l) DH=-a kJ��mol��1
C����ⱥ��ʳ��ˮ���ռ�������ӽ���Ĥ�����ɷ�ֹ�����Ҳ�����Cl2����������
D����⾫��ͭʱ��ͬһʱ���������ܽ�ͭ����������������ͭ������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ������ʡ��УЭ���������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ����
A���ϳɰ����������н�NH3Һ�����룬�ɼӿ�����Ӧ���ʣ����N2��H2��ת����
B����1 mol Ba(OH)2��ϡ��Һ�ͺ�1 mol H2SO4��ϡ��Һ��Ӧ�ͷ�����akJ�����ʾ�÷�Ӧ�к��ȵ��Ȼ�ѧ��Ӧ����ʽΪ��
OH��(aq)��H��(aq)=H2O(l) ∆H = -a kJ��mol��1
C����⾫��ͭʱ��ͬһʱ���������ܽ�ͭ����������������ͭ������С
D������2HI(g)  H2(g)+I2(g)ƽ����ϵ������ƽ����ϵ��ѹǿ��ʹ��ɫ���������������ԭ�����͡�
H2(g)+I2(g)ƽ����ϵ������ƽ����ϵ��ѹǿ��ʹ��ɫ���������������ԭ�����͡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�꽭��ʡ������ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ���� ( )
A���ϳɰ����������н�NH3Һ�����룬�ɼӿ�����Ӧ���ʣ����N2��H2��ת����
B����1 mol Ba(OH)2��ϡ��Һ�ͺ�1 mol H2SO4��ϡ��Һ��Ӧ�ͷ�����akJ�����ʾ�÷�Ӧ�к��ȵ��Ȼ�ѧ��Ӧ����ʽΪ��OH��(aq)��H��(aq)=H2O(l) H = -a kJ��mol��1
C����⾫��ͭʱ��ͬһʱ���������ܽ�ͭ���������ܱ���������ͭ������С
D������2HI(g)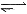 H2(g)+I2(g)ƽ����ϵ������ƽ����ϵ��ѹǿ��ʹ��ɫ���������������ԭ�����͡�
H2(g)+I2(g)ƽ����ϵ������ƽ����ϵ��ѹǿ��ʹ��ɫ���������������ԭ�����͡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ���㽭ʡ�����и�����ѧ��������У������ѧ�Ծ� ���ͣ�ѡ����
���л�ѧ�����ʾ��ȷ����
A��NaH����ˮ��Ӧ�ķ���ʽ��NaH+D2O=NaOH +D2��
B�����������ĵ���ʽ��
C����1 mol Ba(OH)2��ϡ��Һ�ͺ�1 mol H2SO4��ϡ��Һ��Ӧ�ͷ�����akJ�����ʾ�÷�Ӧ�к��ȵ��Ȼ�ѧ��Ӧ����ʽΪ��OH��(aq)��H��(aq)=H2O(l) H=-a kJ��mol��1
D������������Һ��ͨ�������Ķ�����̼�����ӷ�Ӧ����ʽ��
ClO_ + CO2+ H2O= HClO + HCO3_ ��֪����ƽ�ⳣ����K(H2CO3)��K(HClO)��K(HCO3��)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com