
【题目】乙醇是重要的有机化工原料,可由乙烯气相直接水合法生产。气相直接合成的反应为:C2H4(g)+H2O(g)![]() C2H5OH(g) ΔH,乙烯的平衡转化率随温度、压强的变化关系如下图[其中n(C2H4):n(H2O)=1︰1]。
C2H5OH(g) ΔH,乙烯的平衡转化率随温度、压强的变化关系如下图[其中n(C2H4):n(H2O)=1︰1]。
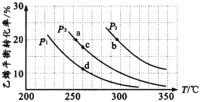
(l)P2时,若起始n(H2O)=n(C2H4)=lmol,容器体积为1L,反应经5 min达到a点,在0~5 min时段,反应速率v(C2H5OH)为____mol/(Lmin),a点的平衡常数Ka=______(保留两位小数)。
(2)乙烯气相直接水合反应的ΔH____0(填“>”或“<”),相同起始量达到a、b所需要的时间ta__tb(填“>”、“<”或“=”,后同)。c、d两点的平衡常数Kc____Kd。
(3)300℃时,要提高乙烯的平衡转化率可采取的措施有______、______ 、___。
【答案】0.04 0.31 < > = 增大压强 增大H2O的浓度[或增大n(H2O) 与n(C2 H4)投料比] 及时分离出生成的乙醇
【解析】
根据化学反应速率的计算公式及平衡常数的表达式进行相关计算;分析图像中乙烯的平衡转化率受温度的影响确定反应是放热反应;根据压强对化学平衡的影响分析压强的大小关系,进一步比较相关的化学反应速率的大小;根据影响化学平衡移动的因素及平衡移动原理选择合适的措施。
(l)P2时,若起始n(H2O)=n(C2H4)=lmol,容器体积为1L,反应经5 min达到a点,由图中信息可知,此时乙烯的转化率为20%,在0~5 min时段,乙烯的变化量为0.2mol,则乙醇的变化量也是0.2mol,反应速率v(C2H5OH)为![]() mol/(Lmin)。a点,C2H4、H2O、C2H5OH的平衡浓度分别为0.8mol/L、0.8mol/L、0.2mol/L,a点的平衡常数Ka=
mol/(Lmin)。a点,C2H4、H2O、C2H5OH的平衡浓度分别为0.8mol/L、0.8mol/L、0.2mol/L,a点的平衡常数Ka=![]() 。
。
(2)由图中信息可知,乙烯的平衡转化率随着温度的升高而减小,说明温度升高该平衡向逆反应方向移动,故乙烯气相直接水合反应的ΔH<0。C2H4(g)+H2O(g)![]() C2H5OH(g)该反应正反应方向是气体分子数减小的方向,压强越大,乙烯的平衡转化率越大,由图中信息可知,在相同温度下,P3的转化率大于P2,则P3的压强较大,b点的温度、压强都比a点大,温度越高、压强越大,化学反应速率越大,达到平衡所用的时间越短,因此,相同起始量达到a、b所需要的时间ta>tb。c、d两点对应的温度相同,因为平衡常数只受温度影响,则平衡常数Kc=Kd。
C2H5OH(g)该反应正反应方向是气体分子数减小的方向,压强越大,乙烯的平衡转化率越大,由图中信息可知,在相同温度下,P3的转化率大于P2,则P3的压强较大,b点的温度、压强都比a点大,温度越高、压强越大,化学反应速率越大,达到平衡所用的时间越短,因此,相同起始量达到a、b所需要的时间ta>tb。c、d两点对应的温度相同,因为平衡常数只受温度影响,则平衡常数Kc=Kd。
(3)300℃时,要提高乙烯的平衡转化率,应设法让化学平衡向正反应方向移动,根据平衡移动原理可知,可采取的措施有:增大压强、增大H2O的浓度[或增大n(H2O) 与n(C2H4)投料比]、及时分离出生成的乙醇。


科目:高中化学 来源: 题型:
【题目】莫沙朵林是一种镇痛药,它的合成路线如下:
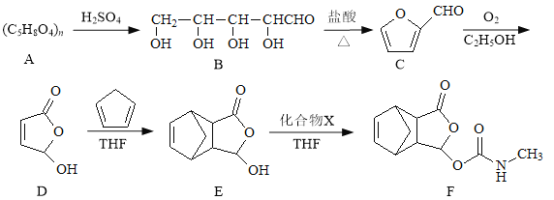
(1)B中手性碳原子数为_________________;化合物C中无氧官能团的名称为_________________。
(2)下列说法正确的是_________________。
A.B与葡萄糖是同系物关系
B.A→B是水解反应
C.E可以发生消去反应,F可与HC1反应
(3)C与银氨溶液反应的化学方程式为_________________。
(4)写出同时满足下列条件的E的同分异构体任意一种结构简式:_________________。
I.核磁共振氢谱有4个峰;
Ⅱ.能发生银镜反应和水解反应;
Ⅲ.能与FeCl3溶液发生显色反应。
(5)已知E+X→F为加成反应,化合物X的结构简式为_________________。
(6)已知: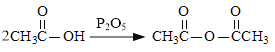 。化合物
。化合物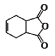 是合成抗病毒药阿昔洛韦的中间体,若以
是合成抗病毒药阿昔洛韦的中间体,若以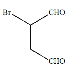 和
和![]() 为原料合成该化合物。请按要求完成下列转化过程:
为原料合成该化合物。请按要求完成下列转化过程: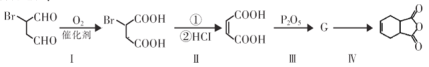
①第I步的反应类型_________________。
②上述步骤Ⅱ中①的反应条件_________________。
③第Ⅲ步中G的结构简式_________________。
④第Ⅳ步的化学方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应2SO2(g)+O2(g)2SO3(g)的描述正确的是( )
A.使用催化剂,SO2的平衡转化率增大
B.增大O2浓度,平衡常数K增大
C.当2![]() 正(SO2)=
正(SO2)=![]() 逆(O2)时,反应达到平衡状态
逆(O2)时,反应达到平衡状态
D.升高温度,反应物中活化分子百分数提高,反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.升高H2SO4稀溶液温度,溶液中c(OH-)增大
B.pH=3的CH3COOH溶液加入CH3COONa固体,溶液的pH减小
C.NaClO稀溶液中加入NaClO固体,溶液中![]() 增大
增大
D.向AgCl、Ag2CrO4的饱和溶液中加入少量AgNO3固体,溶液中![]() 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.10mol/L CH3 COOH溶液滴定10.00mL浓度均为0.10 mol/L NaOH和NH3·H2O的混合液,混合溶液的相对导电能力随乙酸滴入的变化曲线如下图所示。已知:Ka(CH3COOH)=1. 8×10-5,Kb( NH3·H2O) =1. 8× l0-5。下列叙述错误的是
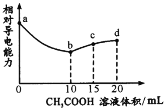
A.ab段为CH3COOH与NaOH的中和过程
B.b点水的电离程度最大
C.c点3c(Na+)=2c(CH3 COOH)+2c(CH3 COO-)
D.d点c(Na+)>c(NH![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )
A.24g镁与27g铝中,质子数之比为12∶13
B.相同质量的16O2和18O2,体积比为9∶8
C.将1LCmol·L-1氯化钠溶液加入水中稀释为5L,得到0.2Cmol·L-1氯化钠溶液
D.同温同压时,H2和CH4两种气体的密度之比为1∶8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究外界条件对反应:mA(g) +nB(g)![]() cZ(g) △H的影响,以A和B物质的量之比为 m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是( )
cZ(g) △H的影响,以A和B物质的量之比为 m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是( )
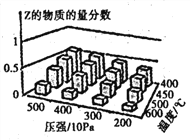
A.在恒温恒容条件下,向已达到平衡的体系中加入少量Z,平衡正向移动,Z的含量增大
B.升高温度,正、逆反应速率都增大,平衡常数增大
C.△H<0 m + n >c
D.△H>0 m +n<c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某矿石的主要成分是BaCO3(含Ca2+、Mg2+、Fe3+等杂质)。实验室利用该矿石制备BaCl2·2H2O的流程如图:
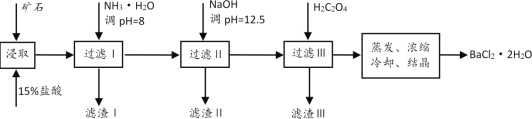
(1)用稀盐酸浸取前需充分研磨矿石,目的是__。
(2)加入NH3·H2O调节pH=8可除去__(填离子符号),滤渣Ⅱ中含__(填化学式)。
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
(3)要使Ca2+完全沉淀,应控制溶液中的![]() 的浓度不低于__mol/L(离子浓度小于1×10-5mol/L时,认为沉淀就达完全);同时加入H2C2O4时又应避免过量,原因是__。(已知:KSP(BaC2O4=1.6×10-7,KSP(CaC2O4=2.3×10-9)。
的浓度不低于__mol/L(离子浓度小于1×10-5mol/L时,认为沉淀就达完全);同时加入H2C2O4时又应避免过量,原因是__。(已知:KSP(BaC2O4=1.6×10-7,KSP(CaC2O4=2.3×10-9)。
(4)利用氧化还原滴定法可测定H2C2O4的浓度,取20.00mLH2C2O4溶液于锥形瓶中,用0.10mol/L酸性KMnO4溶液滴定,KMnO4溶液应装在__(填“酸式滴定管”或“碱式滴定管”)中。写出反应的离子方程式为__。滴定终点的现象为__。若滴定达到终点时,消耗KMnO4溶液30.00mL,则H2C2O4溶液的浓度为__mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,4.48 L己烷含有的分子数为0.2NA
B.15 g甲醛(HCHO)和乙酸的混合物中氧原子数为0.5NA
C.8.8 g乙酸乙酯中含共用电子对的数目为1.3NA
D.1 mol甲基(—14CD3)所含的中子数和电子数分别为11NA、10NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com