
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | | | |||||
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | | ⑦ | | ⑧ | ⑨ |
| 4 | ⑩ | | | | | | | |
| 电离能I(eV) | A | B | C | D | E |
| I1 | 11.3 | 13.6 | 5.2 | 7.6 | 6.0 |
| I2 | 24.4 | 35.1 | 49.3 | 15.0 | 18.8 |
| I3 | 47.9 | 54.9 | 71.6 | 80.1 | 28.4 |
| I4 | 64.5 | 77.4 | 98.9 | 109.2 | 112.0 |
| I5 | 392.1 | 113.9 | 138.3 | 141.3 | 153.7 |




科目:高中化学 来源:不详 题型:单选题
| A.3p能级有一个空轨道的基态原子和核外电子的排布为1s22s22p63s23p2的原子 |
| B.2p能级无空轨道,且有一个未成对电子的基态原子和原子的最外层电子排布为2s22p5的原子 |
| C.M层全充满而N层为4s2的原子和核外电子排布为1s22s22p63s23p64s2的原子 |
D.最外层电子数是核外电子总数的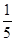 的原子和最外层电子排布为4s24p5的原子 的原子和最外层电子排布为4s24p5的原子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.核外电子是分层运动的 |
| B.所有电子在同一区域里运动 |
| C.能量高的电子在离核近的区域运动 |
| D.不同能量的电子在核外运动占有的区域形状可能不同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X是钠元素 |
| B.离子半径X+>Z2- |
| C.同族元素中Z的氢化物稳定性最强 |
| D.同周期元素中Y的非金属性最强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 相关信息 |
| X | X的基态原子核外的三个能级上电子数相等 |
| Y | Y与X同周期,Y基态原子p能级的成对电子数与未成对电子数相等 |
| Z | Z的单质是一种银白色活泼金属,在空气中燃烧后生成淡黄色的固体 |
| W | 向含W2+的溶液中滴加强碱,其白色氢氧化物在空气中迅速变成灰绿色,最后变成红褐色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X的原子半径比Y小 | B.第一电离能X<Y |
| C.电负性X>Y | D.X和Y的核电荷数之差为m-n |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铍(Be)的氧化物的水化物可能具有两性 |
| B.砹(At)为白色固体,HAt不稳定,AgAt感光性很强 |
| C.硫酸锶(SrSO4)是难溶于水的白色固体 |
| D.硒化氢(H2Se)无色、有毒,比H2S更不稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③ | B.②④ | C.①④ | D.②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com