
| A、c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| B、c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| C、c(HCO3-)=c(Na+)>c(OH-)>c(H+) |
| D、c(OH-)=c(HCO3-)+2c(H2CO3)+c(H+) |
| 0.0224L |
| 22.4L/mol |
| 0.0224L |
| 22.4L/mol |


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
| A、放电时负极区溶液的pH逐渐变大 |
| B、K2Zn(OH)4是还原产物,Ag是氧化产物 |
| C、每生成1 mol K2Zn(OH)4 转移 2 mol 电子 |
| D、该电池正极反应式为:Ag2O2+2 e-+2H2O=2Ag+4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
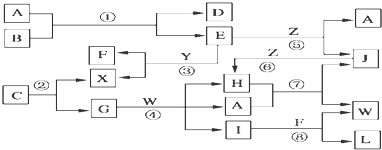
查看答案和解析>>
科目:高中化学 来源: 题型:
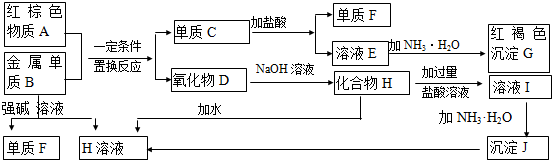
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol?L-1 |
| B、NaHCO3溶液中:c (H+)+c (H2CO3)=c(OH-) |
| C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合气体的压强 |
| B、混合气体的总物质的量 |
| C、气体的平均分子量 |
| D、v(B)=3V(D) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 按如图所示装置进行实验,并回答下列问题:
按如图所示装置进行实验,并回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2,饱和食盐水 |
| B、SO2 氨水 |
| C、NH3,稀盐酸 |
| D、NO2水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com