
 Fe3O4转移电子
Fe3O4转移电子 No
No 

 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:高中化学 来源:物理教研室 题型:013
① 4克Ca变为Ca 2+失去的电子数目为0.1N
② 在标准状况下,40克SO2所占的体积约为11.2升
③ 16克甲烷所含的电子数是10N
④ 1.6克NH2- 离子中含有的电子数为 N
A.①、② B.②、④
C.②、③ D.③、④
查看答案和解析>>
科目:高中化学 来源:山东省胜利油田一中2012届高三下学期第一次调研考试化学试题 题型:013
|
设N为阿伏加德罗常数的值,常温条件下,下列说法正确的是 | |
| [ ] | |
A. |
pH=13的NaOH溶液中OH-离子数目为0.1 N |
B. |
1 L 0.1 mol·L-1的氨水中OH-离子数目为0.1 N |
C. |
I L pH=1的H2SO4溶液中H+离子数目为0.1 N |
D. |
1 L 0.1 mol·L-1的NH4NO3溶液中NH4+离子数目为0.1 N |
查看答案和解析>>
科目:高中化学 来源:2013届河南省西华一高高三上学期第一次月考化学试卷(解析版) 题型:选择题
设N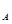 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
A.4.6 g组成为 的有机物,所含C—H键数目一定为0.6N
的有机物,所含C—H键数目一定为0.6N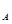
B.8.7 g 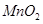 与40 mL 10
与40 mL 10  的浓盐酸充分反应,生成的氯气分子数为0.1N
的浓盐酸充分反应,生成的氯气分子数为0.1N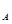
C. 1 mol 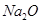 中含有的阴、阳离子总数是3N
中含有的阴、阳离子总数是3N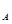 而1 mol
而1 mol  中含有的阴、阳离子总数是4N
中含有的阴、阳离子总数是4N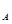
D.在反应

 ↑
↑ 中,每生成4 mol
中,每生成4 mol  转移电子数为15N
转移电子数为15N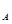
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河南省西华一高高三上学期第一次月考化学试卷(带解析) 题型:单选题
设N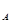 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
A.4.6 g组成为 的有机物,所含C—H键数目一定为0.6N 的有机物,所含C—H键数目一定为0.6N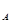 |
B.8.7 g  与40 mL 10 与40 mL 10  的浓盐酸充分反应,生成的氯气分子数为0.1N 的浓盐酸充分反应,生成的氯气分子数为0.1N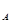 |
C.1 mol 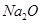 中含有的阴、阳离子总数是3N 中含有的阴、阳离子总数是3N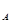 而1 mol 而1 mol 中含有的阴、阳离子总数是4N 中含有的阴、阳离子总数是4N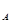 |
D.在反应   ↑ ↑ 中,每生成4 mol 中,每生成4 mol  转移电子数为15N 转移电子数为15N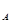 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com