
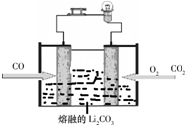
 定”).
定”).| 1-x |
| 2a-x |
| 1 |
| 6 |
| 4 |
| 5 |
| x?x |
| (a-x)?(2a-x) |
| 8 |
| 3 |
| 8 |
| 3 |


科目:高中化学 来源: 题型:
| A、①③④⑧ | B、①②⑥⑨ |
| C、③⑤⑥⑦ | D、①③④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:

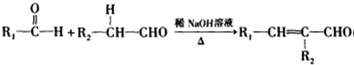 (R1、R2为烃基或氢原子);
(R1、R2为烃基或氢原子); (R1、R2为烃基)
(R1、R2为烃基)查看答案和解析>>
科目:高中化学 来源: 题型:
 )是有机工业的重要原料,可用于合成多种有机物.
)是有机工业的重要原料,可用于合成多种有机物.
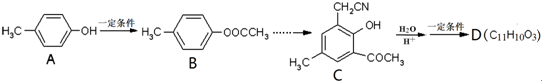
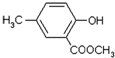 ,合成路线流程图为:
,合成路线流程图为: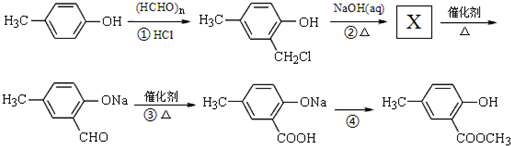
 的合成路线流程图表示(有机物用结构简式,注明反应试剂和条件)
的合成路线流程图表示(有机物用结构简式,注明反应试剂和条件)| 反应试剂 |
| 反应条件 |
| 反应试剂 |
| 反应条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
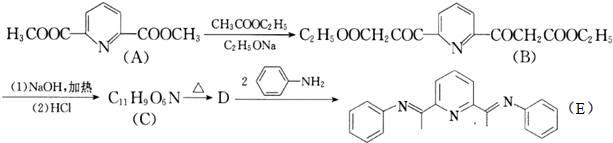
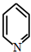 )且环上只有2个取代基;
)且环上只有2个取代基;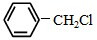 和
和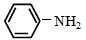 为原料合成西佛碱N-苯基苯甲亚胺(
为原料合成西佛碱N-苯基苯甲亚胺(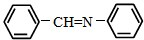 ),请你拟出合成路线:
),请你拟出合成路线:查看答案和解析>>
科目:高中化学 来源: 题型:

| ①O2 |
| ②ZnH2O |
 是一种合成药物的中间体,请写出以CH2(COOH)2、CH2Cl2 及
是一种合成药物的中间体,请写出以CH2(COOH)2、CH2Cl2 及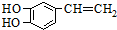 为原料制备该化合物,合成该化合物路线流程图(无机试剂任用),
为原料制备该化合物,合成该化合物路线流程图(无机试剂任用),| 反应试剂 |
| 反应条件 |
| 反应试剂 |
| 反应条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
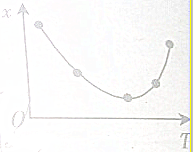 在某恒容密闭容器中通入一定量的二氧化氮,发生反应:2NO2(g)?N2O4(g),测定体系中x随着反应温度(T)变化的关系如图所示,下列关于x说法正确的是( )
在某恒容密闭容器中通入一定量的二氧化氮,发生反应:2NO2(g)?N2O4(g),测定体系中x随着反应温度(T)变化的关系如图所示,下列关于x说法正确的是( )| A、表示二氧化氮的转化率 |
| B、表示二氧化氮的体积分数 |
| C、表示该反应的平衡常数 |
| D、表示该密闭容器混合气体的密度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 次数 | 1 | 2 | 3 | 4 |
| 加入氢氧化钠溶液的质量(g) | 25 | 25 | 25 | 25 |
| 生成沉淀的质量(g) | 2.9 | X | 8.7 | 8.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
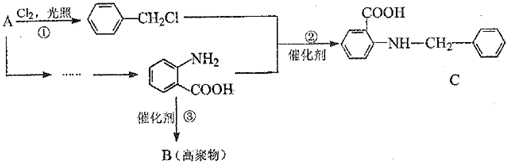
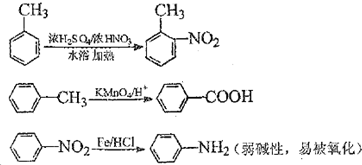
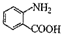 中官能团的名称
中官能团的名称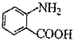 分子与一个α-氨基丙酸分子反应能生成的有机物的结构简式是
分子与一个α-氨基丙酸分子反应能生成的有机物的结构简式是 的同分异构体的结构简式
的同分异构体的结构简式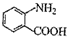 的合成路线.(提示:①合成过程中无机试剂任选;②合成路线表示方法示例如图:C2H5OH
的合成路线.(提示:①合成过程中无机试剂任选;②合成路线表示方法示例如图:C2H5OH| 浓硫酸 |
| 170℃ |
| Br2 |
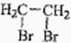 )
)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com