
| A. | 汽油 | B. | 煤 | C. | 石油 | D. | 氢气 |
分析 煤、石油和天然气属于三大化石燃料,都属于不可再生的能源.煤炭中有碳、氢、硫等元素,因此燃烧时生成的烟尘和二氧化硫都会污染空气;石油中有碳、氢、氮、硫等元素,从石油中分馏出汽油和航空煤油燃烧,都会污染空气.氢能源的最大优点是:生成物是水,不污染环境.
解答 解:A.石油中有碳、氢、氮、硫等元素,从石油中分馏出汽油和航空煤油燃烧,都会污染空气,故A错误;
B.煤炭中有碳、氢、硫等元素,因此燃烧时生成的烟尘和二氧化硫都会污染空气,故B错误;
C.石油中有碳、氢、氮、硫等元素,燃烧会污染空气,故C错误;
D.氢能源的最大优点是:生成物是水,不污染环境,属于“绿色能源”,故D正确.
故选D.
点评 本考点属于有关能源的问题,难度不大,节约化石能源,合理的开发新能源是科学家们正在研究的新课题.


科目:高中化学 来源: 题型:选择题
| A. | O2分子间存在着非极性共价键 | |
| B. | CO2分子内存在着极性共价键 | |
| C. | SO2与H2O反应的产物是离子化合物 | |
| D. | 盐酸中含有H+和Cl-,故HCl为离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极为Fe、负极为Fe,电解质溶液为FeCl3溶液 | |
| B. | 正极为Ag、负极为Fe,电解质溶液为CuSO4溶液 | |
| C. | 正极为Fe、负极为Zn,电解质溶液为Fe2(SO4)3溶液 | |
| D. | 正极为C、负极为Fe,电解质溶液为Fe(NO3)3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 吸热反应一定是非自发的化学反应,放热反应不需要加热就能发生反应 | |
| B. | 其它条件不变时,增大压强可以增大活化分子百分数,使化学反应速率加快 | |
| C. | 温度、压强一定时,熵增加的反应都能自发进行 | |
| D. | 应用盖斯定律,可计算某些难以直接测量的反应焓变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
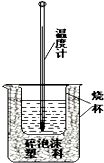 实验室利用如图装置进行中和热的测定.回答下列问题:
实验室利用如图装置进行中和热的测定.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a和b可形成气态化合物 | |
| B. | c的原子半径小于d的原子半径 | |
| C. | b和c形成的化合物为离子化合物 | |
| D. | a和d最高价氧化物的水化物均呈酸性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com