
将10.7gMg、Al和Fe组成的合金溶于足量的氢氧化钠溶液中,产生标准状况下3.36L气体。另取等质量的合金溶于过量盐酸中,生成标准状况下7.84L气体,向反应后的溶液中加入过量NaOH溶液,得到沉淀物质的量为
A. 0.1mol B. 0.2mol C.0.25mol D. 0.3mol
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
一定量的浓硝酸和1.92 g的铜反应,随着铜的不断减少,反应生成的气体颜色逐渐变浅,当铜反应完全时,共收集到气体1.12 L(标准状况),反应中消耗硝酸的物质的量是多少?
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示装置 制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是 ( )
制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是 ( )
|
| 气体 | a | b | c |
| A | NO2 | 浓硝酸 | 铜片 | 浓硫酸 |
| B | SO2 | 浓硫酸 | Fe | 浓硫酸 |
| C | NH3 | 浓氨水 | 生石灰 | 碱石灰 |
| D | Cl2 | 浓盐酸 | MnO2粉末 | 浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
右图为香芹酮分子的结构,下列有关叙述正确的是
A.香芹酮化学式为C9H12O
B.香芹酮可以发生加成反应、消去反应和氧化反应
C.香芹酮能使酸性KMnO4溶液退色
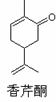 D.香芹酮分子中有3种官能团
D.香芹酮分子中有3种官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
电石(CaC2)发生如下反应合成尿素[CO(NH2)2],可进一步合成三聚氰胺。


(1)CO(NH2)2分子中含有σ键的个数为______。CaCN2中阴离子为CN22-,与CN22-离子互为等电子体的分子的化学式为_______,可推知CN22-的空间构型为_________。
 (2)三聚氰胺在动物体内可转化为三聚氰酸(
(2)三聚氰胺在动物体内可转化为三聚氰酸(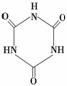 ),三聚氰酸分子中N原子采取______杂化。三聚氰胺与三聚氰酸的分子相互之间通过________结合,在肾脏内易形成结石。
),三聚氰酸分子中N原子采取______杂化。三聚氰胺与三聚氰酸的分子相互之间通过________结合,在肾脏内易形成结石。
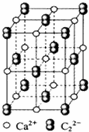
(3)右图是电石的晶胞示意图,则一个晶胞中含有___个Ca2+离子,
研究表明,C22-的存在使晶胞呈长方体,该晶胞中一个Ca2+周围
距离相等且最近的C22-有___个。
查看答案和解析>>
科目:高中化学 来源: 题型:
工厂中用稀硫酸浸泡某矿石后的溶液中,除了含有大量硫酸外,还含有少量NH4+、Fe3+、AsO43-、Cl-。为除去杂质离子,部分操作流程如下:
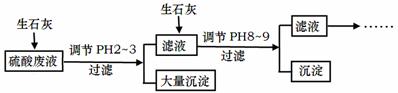
请回答问题:
(1)用稀硫酸浸泡某矿石后的溶液中,硫酸的浓度为4.9g·L-1,则该溶液中的pH约为 。
(2)NH4+在用稀硫酸浸泡某矿石后的溶液中以(NH4)2SO4和NH4Cl形式存在。现有一份(NH4)2SO4溶液,一份NH4Cl溶液,(NH4)2SO4溶液中c(NH4+)恰好是NH4Cl溶液中c(NH4+)的2倍,则c[(NH4)2SO4] c(NH4Cl)(填:<、=或>)。
(3)随着向废液中投入生石灰(忽略溶液温度的变化),溶液中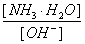 _______(填“增大”、“减小”或“不变”)。
_______(填“增大”、“减小”或“不变”)。
(4)投入生石灰调节pH到2~3时,大量沉淀主要成分为CaSO4·2H2O[含有少量Fe(OH)3],提纯CaSO4·2H2O的主要操作步骤:向沉淀中加入过量 ,充分反应后,过滤、洗涤、 。
(5)25℃, H3AsO4电离常数为K1=5.6×10-3,K2=1.7×10-7,K3=4.0×10-12。当溶液中pH调节到8~9时,沉淀主要成分为Ca3(AsO4)2。
①pH调节到8左右Ca3(AsO4)2才开始沉淀的原因是 。
②Na3AsO4第一步水解的平衡常数数值为: 。
③已知:AsO43-+2I-+2H+= AsO33-+I2+H2O ,SO2+I2+2H2O=SO42-+2I-+4H+ 。上述两个反应中还原性最强的微粒是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列反应中,硝酸既表现氧化性又表现酸性的是 ( )
A.FeO和HNO3 B.Al (OH)3与HNO3
(OH)3与HNO3
C.H2S和HNO3 D.NH3与HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化钙可以用于改善地表水质,处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。工业上生产过氧化钙的主要流程如下:

已知CaO2·8H2O呈白色,微溶于水,加热至350 ℃左右开始分解放出氧气。
(1)用上述方法制取CaO2·8H2O的化学方程式是______________________________;
(2)检验“水洗”是否合格的方法是___________________________________________;
(3)沉淀时常用冰水控制温度在0 ℃左右,其可能原因是______________________;
(4)测定产品中CaO2的含量的实验步骤:
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol·L-1的H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。
第三步:逐滴加入浓度为c mol·L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL。
【已知:I2+2S2O32-=2I-+S4O62-】
①第一步发生的反应的化学方程式为 ;
CaO2的质量分数为____________(用字母表示);
②某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能________(填“不受影响”、“偏低”或“偏高”),原因是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将等物质的量的镁和铝混合,取等质量该混合物四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是 ( )
A.3 mol·L-1 HCl B.4 mol·L-1 HNO3
C.8 mol·L-1 NaOH D.18 mol·L-1 H2SO4
mol·L-1 H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com