
【题目】含氯的物质与人们的生活密切相关。已知氯元素常见的化合价有-1、0、+1、+3、+5、+7六种,其不同价态的物质间可相互转化。回答下列问题:
(1)氯原子的原子结构示意图___;氯离子的电子式___。
(2)氯气能使湿润的有色布条褪色,起到漂白作用的物质是____(写名称),漂粉精的主要有效成分是___(写化学式)。
(3)实验室制取氯化氢的化学方程式____。
(4)工业上将含有氯气的尾气通过___进行处理,在处理时发生的反应中氯气作为____。
a.氧化剂 b.还原剂 c.既是氧化剂又是还原剂 d.既不是氧化剂又不是还原剂
(5)写出氯气的两种用途____、____。
【答案】
![]() 次氯酸 Ca(ClO)2 NaCl+H2SO4
次氯酸 Ca(ClO)2 NaCl+H2SO4![]() NaHSO4+HCl↑ NaOH溶液 c 制盐酸 漂白粉
NaHSO4+HCl↑ NaOH溶液 c 制盐酸 漂白粉
【解析】
(1)氯原子是17号元素,核外电子分为三个电子层,第一层2个电子,第二层8个电子,第三层7个电子,原子结构示意图为 ;氯离子为阴离子,原子周围有8个电子,氯离子的电子式为:
;氯离子为阴离子,原子周围有8个电子,氯离子的电子式为:![]() ;
;
故答案为: ;
;![]() ;
;
(2)氯气与水反应生成HClO,HClO有漂白性,则氯气能使湿润的有色布条褪色,起到漂白作用的物质是次氯酸;漂粉精的主要有效成分是次氯酸钙,其化学式为Ca(ClO)2;
故答案为:次氯酸;Ca(ClO)2;
(3)实验室制备氯化氢气体利用原料氯化钠和浓硫酸加热反应生成氯化氢,微热时生成硫酸氢钠和氯化氢,反应的化学方程式为:NaCl+H2SO4![]() NaHSO4+HCl↑,
NaHSO4+HCl↑,
故答案为:NaCl+H2SO4![]() NaHSO4+HCl↑;
NaHSO4+HCl↑;
(4)氯气是有毒气体,能与氢氧化钠溶液反应,氯气用氢氧化钠溶液吸收;氯气与NaOH反应时,Cl元素的化合价既升高又降低,所以氯气既是氧化剂又是还原剂;
故答案为:NaOH溶液;c;
(5)氯气是一种有着广泛用途的重要化工原料,可用于制盐酸、漂白粉、有机溶剂与多种农药,
故答案为:制盐酸;漂白粉。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】对于可逆反应:mA(g)+nB(g) ![]() pC(g)+qD(g)(m、n、p、q均为化学计量数),根据图示曲线回答:
pC(g)+qD(g)(m、n、p、q均为化学计量数),根据图示曲线回答:
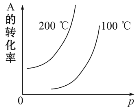
(1)正反应是___热反应。
(2)m+n___p+q(填“>”“<”或“=”)。
(3)若将纵坐标A的转化率换成A在平衡混合物中的质量分数,则逆反应是____ 热反应,m+n___p+q(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是101 kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )
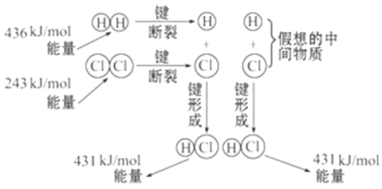
A. 1 mol H2中的化学键断裂时需要吸收436 kJ能量
B. 2 mol HCl分子中的化学键形成时要释放862 kJ能量
C. 此反应的热化学方程式为:H2(g)+Cl2(g)==2HCl(g)ΔH=+183 kJ/mol
D. 此反应的热化学方程式为:1/2H2(g)+1/2Cl2(g)==HCl(g)ΔH=-91.5 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种微粒的结构示意如下,下列说法错误的是( )

A.它们属于不同种元素
B.它们的核外电子排布相同
C.它们都是离子
D.它们都具有稀有气体原子的稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有机物的描述正确的是
A. 组成为C6H14的烷烃中仅能由1种单炔烃加氢而制得的结构有2种
B. 立方烷( ![]() )燃烧的现象与乙烷燃烧的现象相同
)燃烧的现象与乙烷燃烧的现象相同
C. ![]() 分子中所有原子不可能处于同一平面
分子中所有原子不可能处于同一平面
D. 用碳酸钠溶液不能一次性鉴别乙酸、苯和乙醇三种无色液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。回答下列问题:
(1)SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式_______________________________。
(2)SiHCl3在催化剂作用下发生反应:
2SiHCl3(g)=SiH2Cl2(g)+ SiCl4(g) ΔH1= +48 kJ·mol1
3SiH2Cl2(g)=SiH4(g)+2SiHCl3 (g) ΔH2= 30 kJ·mol1
则反应4SiHCl3(g)=SiH4(g)+ 3SiCl4(g)的ΔH=__________ kJ·mol1。
(3)对于反应2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。

①343 K时反应的平衡转化率α=_________%。平衡常数K343 K=__________(保留2位小数)。
②在343 K下:要提高SiHCl3转化率,可采取的措施是___________;要缩短反应达到平衡的时间,可采取的措施有____________、___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种金属组成的合金25克与氯气完全反应,共用去标况下氯气11.2升,该合金的可能组成是
A.Na和MgB.Cu和CaC.Cu和ZnD.Fe和Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在人类的生活生产中有着重要的作用,Fe2+、Fe3+是影响水质的一个重要因素。回答下列问题:
I:测量某河水样本中铁的含量
(1)水样中Fe2+的含量越大,溶解氧的含量就越低,用离子方程式解释原因___________。
(2)测定Fe2+取5mL c mo/L的KMnO4标准液,稀释至100mL。取10.00mL河水水样,加入稀硫酸后,用稀释后的KMnO4溶液进行滴定,用去KMnO4溶液V1mL。
①用___________(填滴定管的名称)盛放KMnO4标准液。
②滴定达到终点的标志是___________。
(3)测定Fe3+:取10.00mL水样,转移至盛有过量锌粒的烧杯中充分反应。加入过量稀硫酸,用表面皿盖住烧杯并加热10分钟。冷却后用(2)中稀释后的KMnO4溶液滴定,消耗KMnO4溶液V2mL。
①锌粒的作用是___________。
②河水中Fe3+的浓度是___________mol/L(用含字母的代数式表示)。
Ⅱ:氢氧化亚铁[Fe(OH)2]在常温常压下为白色固体。
(4)当溶液中的离子浓度<1×10-5mol·L-1时,可以认为该离子已沉淀完全。已知常温Fe(OH)2的Ksp为8.0×10-16。现调节含Fe2+的某河水样品pH=9,用简要计算过程说明Fe2+是否已经达到沉淀完全:___________。
(5)一种用Na2SO4溶液做电解液,电解制取Fe(OH)2的实验装置如图所示。通电后,溶液中产生白色沉淀,且较长时间不变色。
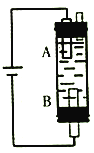
①必须使用铁电极的是___________(填“A"或“B”)极。
②B电极的电极反应式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某抗肿瘤药物中间体的合成路线如下。下列说法正确的是( )

A. 吲哚的分子式为C8H6N
B. 苯甲醛中所有原子不可能全部共平面
C. 可用新制氢氧化铜悬浊液区分苯甲醛和中间体
D. 1mol该中间体,最多可以与9mol氢气发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com