
| ʵ�ʲ��� |
| ���۲��� |
| 0.002 |
| 6 |
| 1 |
| 3 |
| 1.55��10 -4 | ||
|



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������������Ӧ������ͬ |
| B���������з�Ӧ��ƽ�ⳣ����ͬ |
| C����������CO�����ʵ������������е��� |
| D����������CO��ת��������������CO2��ת���ʺ�С��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��H+��Ca2+��Na+��CO32- |
| B��Na+��Mg2+��OH-��Cl- |
| C��Fe2+��Mg2+��Cl-��H+ |
| D��Ba2+��Cl-��OH-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��K+�� Na+�� Cl-��NO3- |
| B��Cu2+�� H+�� HCO3-�� Cl- |
| C��Na+�� Ba2+�� Cl-�� SO42- |
| D��Fe2+�� H+�� NO3-�� ClO- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
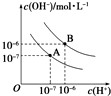 ��֪ˮ��25�棨A����T�棨B��ʱ�������ƽ��������ͼ��ʾ��
��֪ˮ��25�棨A����T�棨B��ʱ�������ƽ��������ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ؼ����Ʊ�����������ˮ���ռ����������ȳ���ƾ��ƣ����Ƴ����� |
| B�����Թܼ���ʱ���ȹ̶��ֲ����ȣ�����Թ����ؾ��ȼ��� |
| C���ڲⶨ��Һ��pHʱ����������ˮʪ���ò�����պȡ��Һ������ֽ�в��������ɫ���Ƚ� |
| D����ȼ��ȼ�����壨��H2��CO��CH4��ʱ���ȼ������崿�ȣ����ȼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| A����H1=��H2=��H3 |
| B��2��H3=��H2����H1 |
| C����H3����H2����H1 |
| D��2|��H3|=|��H2|��|��H1| |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������� | B�����ۢ��� |
| C�����ۢ��� | D�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com