
【题目】在晶体中,微观粒子是有规律排布的。而实际上的晶体与理想结构或多或少会产生偏离,这种偏离称为晶体的缺陷。由于晶体缺陷,氧化铁FexO中的x常常不确定。
(1)请写出铁原子基态电子排布式___________________。
(2)Fe2+与Fe3+相比,较稳定的是___________,请从二者结构上加以解释_______________。
(3)硫氰根离子和异硫氰根离子都可用SCN-表示,碳原子都处于中央,则碳原子的轨道杂化类型为____________________。其中异硫氰根离子与CO2是等电子体,异硫氰根离子的电子式为________________。Fe3+与SCN-可以形成配位数![]() 的配离子,若Fe3+与SCN-以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为_____________。
的配离子,若Fe3+与SCN-以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为_____________。
(4)如图:铁有![]() 、
、![]() 、
、![]() 三种同素异形体,三种晶体在不同温度下能发生转化。
三种同素异形体,三种晶体在不同温度下能发生转化。
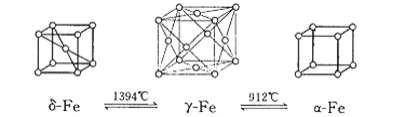
请问:![]() 、
、![]() 、
、![]() 这三种晶胞的棱长之比为:___________。
这三种晶胞的棱长之比为:___________。
【答案】[Ar]3d64s2 Fe3+ Fe3+的电子排布式为[Ar]3d5,Fe2+的电子排布式为[Ar]3d6,Fe3+的3d能级处于半充满状态,是一种较稳定的结构 sp ![]() FeCl3+5KSCN=K2[Fe(SCN)5]+3KCl 2
FeCl3+5KSCN=K2[Fe(SCN)5]+3KCl 2![]() :3
:3![]() :3
:3
【解析】
(1)根据构造原理,书写Fe原子核外电子排布式;
(2)原子核外各个轨道电子数处于全满、半满或全空时是稳定状态;
(3)根据价层电子对理论分析C原子杂化方式;根据等电子体结构相似书写异硫氰根离子的电子式;
(4)根据各自结构的相对位置分析计算。
(1)Fe是26号元素,原子核外有26个电子,根据核外电子排布规律可知铁原子基态电子排布式为[Ar]3d64s2;
(2)Fe3+的电子排布式为[Ar]3d5,Fe2+的电子排布式为[Ar]3d6,Fe3+的3d能级处于半充满状态,是一种较稳定的结构,所以Fe3+比Fe2+稳定;
(3)SCN-中碳原子都处于中央,碳周围有两个![]() 键,没有孤电子对,所以碳原子按sp方式杂化,互为等电子体的粒子结构相似,所以根据CO2分子的结构可判断异硫氰根离子的电子式为
键,没有孤电子对,所以碳原子按sp方式杂化,互为等电子体的粒子结构相似,所以根据CO2分子的结构可判断异硫氰根离子的电子式为![]() ,FeCl3与KSCN在水溶液按1:5反应,反应的化学方程式为FeCl3+5KSCN=K2[Fe(SCN)5]+3KCl;
,FeCl3与KSCN在水溶液按1:5反应,反应的化学方程式为FeCl3+5KSCN=K2[Fe(SCN)5]+3KCl;
(4)设铁原子半径为a,根据晶胞结构图,![]() 晶体中晶胞的棱长为
晶体中晶胞的棱长为![]() ,γ晶体中晶胞的棱长为
,γ晶体中晶胞的棱长为![]() ,
,![]() 晶体中晶胞的棱长为2a,所以三种晶胞的棱长之比为2
晶体中晶胞的棱长为2a,所以三种晶胞的棱长之比为2![]() :3
:3![]() :3。
:3。


科目:高中化学 来源: 题型:
【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
|温度/ ℃ | 700 | 900 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K=____________,△H____0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。则6s时c(A)=_____mol·L-1, C的物质的量为______mol;若反应经一段时间后,达到平衡时A的转化率为_____,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为_________;
(3)判断该反应是否达到平衡的依据为______(填正确选项前的字母):
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等
(4)1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为_____________。
A(g)+B(g)的平衡常数的值为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水的电离平衡曲线如图所示,下列说法正确的是

A.水的离子积常数关系为:KW(B)>KW(A)>KW(C)>KW(D)
B.向水中加入醋酸钠固体,可从C点到D点
C.B点对应的温度下,pH=4的硫酸与pH=10的氢氧化钠溶液等体积混合,溶液的pH=7
D.升高温度可实现由C点到D点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25°C时,Ksp[Mg(OH)2]=5.61×10-12,Ksp[MgF2]=7.42×10-11,下列说法正确的是
A.25°C时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大
B.25°C时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大
C.25°C时,Mg(OH)2固体在20mL 0.01 mol/L氨水中的Ksp比在20mL 0.01mol/L NH4Cl溶液中的Ksp小
D.25°C时,在Mg(OH)2的悬浊液加入浓NaF溶液后,Mg(OH)2不可能转化成为MgF2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ni2+在氨性溶液中和镍试剂(丁二酮肟)反应生成鲜红色的螯合物沉淀,在定性分析中用于鉴定![]() 。该反应可表示为
。该反应可表示为
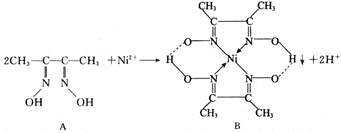
(1)Ni在元素周期表中的位置是_______,其基态原子的未成对电子数是_______。
(2)与Ni同周期,基态原子最外层电子数为1的元素有________(填元素符号)。其中原子序数最大的元素,其基态原子核外电子排布不符合________(填选项字母)。
A.构造原理 B.泡利不相容原理 C.洪特规则
(3)已知丁二酮肟(物质A)通常情况下是白色粉末,熔点238~240℃,溶于乙醇、乙醚,几乎不溶于水。则丁二酮肟的晶体类型是________。
(4)丁二酮肟的组成元素电负性由大到小的顺序是________。
(5)物质B中含有的微粒间作用力类型有________。
A.离子键 B.共价键 C.氢键 D.配位键
(6)物质B中C原子的杂化方式是________。
(7)氧化镍(NiO)的晶体结构为立方晶系,其晶胞结构与氯化钠相似。氧化镍晶胞中,与一个Ni2+紧邻且距离相等的O2-以线段相连,构成的几何图形为________。
(8)某种氧化镍晶体中存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+取代,晶体仍显电中性。实验测得该氧化镍晶体的化学式为Ni0.90O,其晶胞参数为acm,NA代表阿伏加德罗常数的值,则该晶体的密度为________(用含a和NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将0.1molAgCl固体加入1L 0.1mol·L-1Na2CO3溶液中,充分搅拌(不考虑液体体积变化),已知:Ksp(AgCl)=2×10-10;Ksp(Ag2CO3)=1×10-11,下列有关说法正确的是 ( )
A.沉淀转化反应2AgCl(s)+ CO32-(aq)![]() Ag2CO3(s)+2Cl-(aq)的平衡常数为20mol·L-1
Ag2CO3(s)+2Cl-(aq)的平衡常数为20mol·L-1
B.约有2×10-5mol AgCl溶解
C.反应后溶液中的:c(Na+)>c (CO32-) >c (Ag+)>c (Cl-) >c (H+)
D.反应后溶液中的:c(Na+)+ c (Ag+)+ c (H+)="c" (CO32-)+ c (HCO3-)+ c (Cl-) +c (OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】色氨酸是植物体内生长素生物合成重要的前体物质,普遍存在于高等植物中。纯净的色氨酸为白色或微黄色结晶,微溶于水易溶于盐酸或氢氧化钠,其结构如图所示,下列关于色氨酸的说法不正确的是
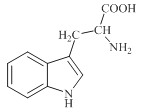
A.色氨酸的分子式为C11H12N2O2
B.色氨酸能发生取代、加成、酯化、中和反应
C.色氨酸微溶于水而易溶于酸或碱溶液是因为其与酸、碱都能反应生成盐
D.将色氨酸与甘氨酸(NH2CH2COOH)混合,在一定条件下最多可形成三种二肽
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸在食品、医药等方面有着广泛用途。一种合成阿魏酸的反应可表示为
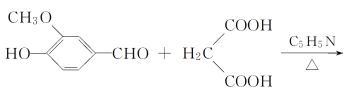
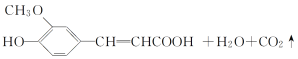
香兰素 丙二酸 阿魏酸
下列说法正确的是( )
A.可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成
B.香兰素、阿魏酸均可与Na2CO3、NaOH溶液反应
C.通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应
D.与香兰素互为同分异构体,分子中有5种不同化学环境的氢,且能发生银镜反应的酚类化合物共有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向CH3COONa稀溶液中加入(或通人)少许X物质,其溶液中部分微粒的浓度变化如表所示(溶液温度不变)。
微粒 | H+ | OH- | CH3COO- | CH3COOH |
物质的量浓度 | 增大 | 减小 | 减小 | 增大 |
X物质是下列物质中的( )
A.氢氧化钠B.蒸馏水C.氯化氢D.磷酸钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com