
已知如图Z4-1所示各物质的转化关系中,某些反应部分产物已被省去。其中反应②用于常见金属 I 的冶炼,B为淡黄色固体,D、G、H 均为气体且 D、H 无色。
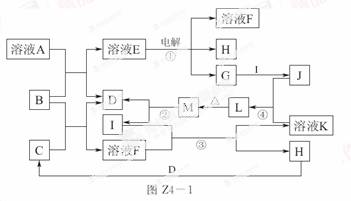
试回答下列问题:
(1)溶液A为________(写名称),B 的电子式________________________。
(2)反应①的离子方程式:____________________,
反应③的离子方程式:_____________________。
(3)有同学认为M也可由溶液J、溶液K各自加热灼烧获得,试判断这种说法是否正确?________(填“是”或“否”),理由是___________________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
节能减排成为社会发展过程中不可回避的问题。下列说法正确的是
①推广乙醇汽油可以减轻环境污染,降低尾气中一氧化碳含量。
②乙醇汽油作为一种新型清洁燃料,是目前世界上可再生能源的发展重点之一。
③乙醇属于可再生资源,使用乙醇汽油可以缓解目前石油紧缺的矛盾。
④太阳能、风能、水能、生物质能、地热能和海洋能等都属于可再生能源。
⑤乙醇属于一级能源
A.①②⑤ B.①②③ C.③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量Fe和Fe2O3的混合物投入250 mL 2 mol/L的硝酸中,反应共生成1.12 L NO(标准状况下),再向反应后的溶液中加入1 mol/L的NaOH溶液,当沉淀完全时所加NaOH溶液的体积最少是( )
A.450 mL B.500 mL C.400 mL D.不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
Cl2是纺织工业中常用的漂白剂,Na2S2O3可作漂白布匹后的“脱氯剂”。 脱氯反应为
S2O32-+Cl2+H2O→SO42-+Cl-+H+(未配平)。下列对该反应的说法不正确的是( )
A.反应中硫元素发生了氧化反应 B.脱氯反应后的溶液显酸性
C.根据该反应可判断还原性:S2O32->Cl- D.反应中每脱去1mol Cl2会生成1 mol SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E均为短周期主族元素,其原子序数依次增大。其中A元素原子核内只有1个质子;A与C,B与D分别同主族; B、D两元素原子序数之和是A、C两元素原子序数之和的2倍。
请回答下列问题:
(1)由上述元素组成的下列物质中属于非电解质的是 (填字母编号)。
a.A2B b.DB2 c.E2 d.C2DB3
(2)D元素在元素周期表中的位置为 ;
化合物CBA中含有的化学键类型是 ;
化合物C2B中两种离子的半径大小关系为 > (填离子符号)。
(3)实验室中欲选用下列装置制取并收集纯净干燥的E2气体。
①实验中应选用的装置为 (按由左到右的连接顺序填写);
②装置A中发生反应的离子方程式为 。
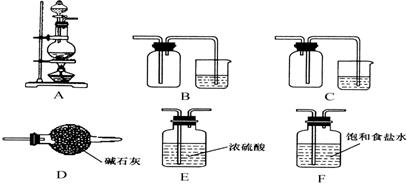
查看答案和解析>>
科目:高中化学 来源: 题型:
右图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4∶5,化合物D是重要的工业原料。
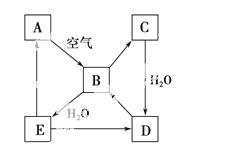
(1)写出A在加热条件下与H2反应的化学方程式:
_________________________________________________________________;
(2)写出E与A的氢化物反应生成A的化学方程式:
_________________________________________________________________;
(3)写出一个由D生成B的化学方程式:
________________________________________________________________;
(4)将5 mL 0.10 mol·L-1的E溶液与10 mL 0.10 mol·L-1的NaOH溶液混合。
①写出反应的离子方程式: _________________________________________;
②反应后溶液的pH________7(填“大于”“小于”或“等于”),理由是______________________________________________________________ ___;
___;
③加热反应后的溶液,其pH________(填“增大”“不变”或“减小”),理由是_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙均为中学化学常见的气体单质,A、B、C为常见的化合物,已知:
⑴A和B都极易溶于水,用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟
⑵各物质之间存在如下图所示的转化关系

请回答下列问题:
⑴写出物质A与B的化学式: 、 。
⑵C溶液中离子浓度的大小关系是 。
⑶“C溶液+镁粉→甲”的化学方程式为 。
⑷丙气体通入200 mL氢氧化钠溶液中恰好完全反应,此时电子转移总数为0.1NA,则氢氧化钠溶液的pH为 。
⑸常温下,向含白色沉淀M的浊液中加入氯化钠固体,M的溶解度将 (填“增大”、“减小”或“不变”),Ksp(M)将 (填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中含有相同的化学键类型的是( )
A.NaCl、HCl、H2O、NaOH
B.Cl2、Na2S、HCl、SO2
C.HBr、CO2、H2O、CS2
D.Na2O2、H2O2、H2O、O3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于浓硫酸的叙述正确的是( )
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.浓硫酸在常温时可以与木炭反应
C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
D.浓硫酸在常温下能够使铁、铝等金属钝化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com