
弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
Ⅰ.已知H2A在水中存在以下平衡:H2AH++HA-,HA-H++A2-。
(1)相同浓度下,NaHA溶液的pH________(填“大于”、“小于”或“等于”) Na2A溶液的pH。
(2)某温度下,若向0.1 mol/L的NaHA溶液中逐滴滴加0.1 mol/L KOH溶液至溶液呈中性。此时该混合溶液中下列关系中,一定正确的是________。
a.c(H+)·c(OH-)=1×10-14
b.c(Na+)+c(K+)=c(HA-)+2c(A2-)
c.c(Na+)>c(K+)
d.c(Na+)+c(K+)=0.05 mol/L
(3)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:
CaA(s)Ca2+(aq)+A2-(aq) ΔH>0。
①降低温度时,Ksp________(填“增大”“减小”或“不变”)。
②滴加少量浓盐酸,c(Ca2+)________(填“增大”“减小”或“不变”)。
Ⅱ.含有Cr2O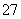 的废水毒性较大,某工厂废水中含5.00×10-3 mol·L-1的Cr2O
的废水毒性较大,某工厂废水中含5.00×10-3 mol·L-1的Cr2O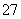 。为使废水能达标排放,作如下处理:Cr2O
。为使废水能达标排放,作如下处理:Cr2O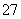
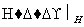 Cr3+、Fe3+石灰水,Cr(OH)3、Fe(OH)3
Cr3+、Fe3+石灰水,Cr(OH)3、Fe(OH)3
(1)该废水中加入绿矾(FeSO4·7H2O)和稀硫酸,发生反应的离子方程式为
________________________________________________________________________。
(2)欲使10 L该废水中的Cr2O 完全转化为Cr3+,理论上需要加入________g FeSO4·7H2O。
完全转化为Cr3+,理论上需要加入________g FeSO4·7H2O。
(3)若处理后的废水中残留的c(Fe3+)=2×10-13 mol·L-1,则残留的Cr3+的浓度为________。(已知:
Ksp=4.0×10-38 Ksp=6.0×10-31)
解析:(2)温度不确定,所以c(H+)·c(OH-)不一定为1×10-14;由电荷守恒可知,c(H+)+c(Na+)+c(K+)=c(HA-)+2c(A2-)+c(OH-),由于溶液呈中性,则c(H+)=c(OH-),c(Na+)+c(K+)=c(HA-)+2c(A2-);若两溶液的体积相同,则是最终溶液为Na2A,呈碱性,所以KOH溶液的体积相对小,等浓度的情况下,必然有c(Na+)>c(K+),c(Na+)+c(K+)也不可能等于0.05 mol/L
答案:Ⅰ.(1)小于 (2)bc (3)①减小 ②增大
Ⅱ.(1)Cr2O +6Fe2++14H+===2Cr3++6Fe3++7H2O (2)83.4 (3)3×10-6 mol·L-1
+6Fe2++14H+===2Cr3++6Fe3++7H2O (2)83.4 (3)3×10-6 mol·L-1


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
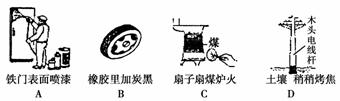
通过控制或改变反应条件可以加快、减缓甚至阻止反应的进行,使化学反应有利于人类的生存和提高生活质量。下列各图所示的措施中,能加快化学反应速率的是( )
查看答案和解析>>
科目:高中化学 来源: 题型:
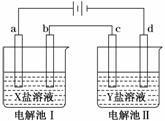
下图所示的电解池Ⅰ和Ⅱ中,a、b、c和d均为Pt电极。电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d。符合上述实验结果的盐溶液是( )
| 选项 | X | Y |
| A | MgSO4 | CuSO4 |
| B | AgNO3 | Pb(NO3)2 |
| C | FeSO4 | Al2(SO4)3 |
| D | CuSO4 | AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行反应:X(g)+3Y(g)2Z(g),有关下列图像的说法不正确的是( )
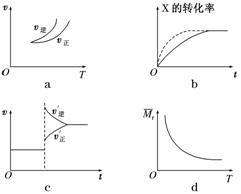
A.依据图a可判断该反应的正反应为放热反应
B.在图b中,虚线可表示使用了催化剂
C.若正反应的ΔH<0,图c可表示升高温度使平衡向逆反应方向移动
D.由图d中气体平均相对分子质量随温度的变化情况,可推知正反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
已知FeCl3溶液与KSCN溶液混合后发生反应FeCl3+3KSCNFe(SCN)3+3KCl,达到平衡后,改变条件,则下列说法正确的是( )
A.向溶液中加入少许KCl固体,溶液颜色变浅
B.升高温度,平衡一定发生移动
C.加入少许KCl固体或者加入少许FeCl3固体平衡常数均发生变化,且变化方向相反
D.平衡常数表达式为K=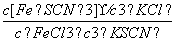
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度和压强下的理想气体,影响其所占体积大小的主要因素是()
| A. | 分子直径的大小 | B. | 分子间距离的大小 | |
| C. | 分子间引力的大小 | D. | 分子数目的多少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素的单质0.1mol与Cl2充分反应后,生成物的质量比原单质的质量增加了10.5g,则这种元素是()
| A. | K | B. | Mg | C. | Al | D. | Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
有一种碘和氧的化合物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,则这种化合物的化学式为()
| A. | I2O4 | B. | I3O5 | C. | I4O7 | D. | I4O9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
C、N、O、Al、Si、Cu是常见的六种元素。
(1)Si位于元素周期表第____周期第_____族。
(2)N的基态原子核外电子排布式为_____;Cu的基态原子最外层有___个电子。
(3)用“>”或“<”填空:
| 原子半径 | 电负性 | 熔点 | 沸点 |
| Al_____Si | N____O | 金刚石_____晶体硅 | CH4____SiH4 |
(4)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。

0-t1时,原电池的负极是Al片,此时,正极的电极反应式是_____,溶液中的H+向___极移动,t1时,原电池中电子流动方向发生改变,其原因是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com