
 原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种类最多的元素之一,Y的基态原子最外层电子数是其内层电子总数的2倍,Z的基态原子2p轨道上有3个未成对电子,W的原子序数为29.
原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种类最多的元素之一,Y的基态原子最外层电子数是其内层电子总数的2倍,Z的基态原子2p轨道上有3个未成对电子,W的原子序数为29.分析 Y的基态原子最外层电子数是其内层电子总数的2倍,最外层电子数为4,内层电子数为2,那么Y是C元素;
X是形成化合物种类最多的元素之一,那么X是H元素;
元素Z基态原子的2p轨道上有3个未成对电子,核外电子排布为1s22s22p3,则Z为N元素;
W的原子序数为29,那么W是Cu元素,
(1)C的单质易形成原子晶体,Cu为金属晶体;
(2)依据C元素和N元素在化合物中常见化合价判断即可;
(3)W的原子序数为29,则W是Cu元素,结合元素、物质的结构和性质分析解答.
解答 解:Y的基态原子最外层电子数是其内层电子总数的2倍,最外层电子数为4,内层电子数为2,那么Y是C元素;
X是形成化合物种类最多的元素之一,那么X是H元素;
元素Z基态原子的2p轨道上有3个未成对电子,核外电子排布为1s22s22p3,则Z为N元素;
W的原子序数为29,那么W是Cu元素,
(1)碳元素易形成原子晶体:金刚石,铜为金属晶体,故答案为:C;Cu;
(2)C元素在化合物中呈现+4价,N元素易形成-3价,故两者形成的化合物为:C3N4,由于C与N的半径比Si要小,故C-N键键能比Si-Si键能大,故硬度比晶体硅大,故答案为:C3N4;大;
(3)合金中原子之间存在金属键,Cu原子处于面心,Au原子处于顶点位置,该晶胞中Cu原子个数=6×$\frac{1}{2}$=3,Au原子个数=8×$\frac{1}{8}$=1,故Cu原子与Au原子数目之比为3:1,根据图知,黑色小球相当于H原子,为8个,所以晶体储氢后的化学式应为H8AuCu3,
故答案为:3:1;金属键;H8AuCu3.
点评 本题以元素的推断为载体,考查了晶体类型的判断、晶胞的计算等,难度中等,侧重对基础知识的巩固,注意对基础知识的理解掌握.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:选择题
| 元素代号 | L | M | X | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A. | R的氧化物对应的水化物可能具有两性 | |
| B. | X单质可在氧气中燃烧生成XO3 | |
| C. | 离子半径大小:r (M3+)>r (T2-) | |
| D. | L2+和X2-的核外电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
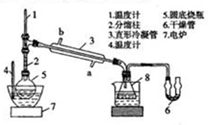 硼酸三甲酯可作溶剂、脱水剂和塑料、油漆、喷漆等的防火剂等.实验室合成硼酸三甲酯的反应、装置示意图及有关数据如下:
硼酸三甲酯可作溶剂、脱水剂和塑料、油漆、喷漆等的防火剂等.实验室合成硼酸三甲酯的反应、装置示意图及有关数据如下:| 硼酸三甲酯 | 甲醇 | |
| 相对分子量 | 104 | 32 |
| 溶解性 | 与乙醚、甲醇混溶,能水解 | 与水混溶 |
| 沸点/℃ | 68 | 64 |
| 备注 | 硼酸三甲酯与甲醇能形成共沸混合物,沸点54℃ | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
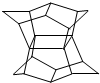 1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图分子,因其形状像东方塔式庙宇(pagoda-style temple),所以该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是( )
1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图分子,因其形状像东方塔式庙宇(pagoda-style temple),所以该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是( )| A. | 分子式为C20H20 | B. | 一氯代物的同分异构体只有四种 | ||
| C. | 分子中含有二个亚甲基(-CH2-) | D. | 分子中含有8个五元碳环 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤⑧ | B. | ④⑤⑦⑧ | C. | ④⑤⑧ | D. | ③④⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Mg2+、SO42- | B. | H+、Mg2+、CO32- | C. | Ag+、NO3-、Cl- | D. | Fe2+、H+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
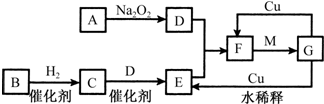
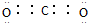 .
.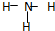 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数 C>B>D>A | B. | 单质熔点 D>B,A>C | ||
| C. | 原子半径 D>B>C>A | D. | 简单离子半径 C>A>D>B |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com