
【题目】向20 mL某物质的量浓度的AlCl3溶液中滴入2 mol·L-1NaOH溶液时,得到的Al(OH)3沉淀质量与所滴加的NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
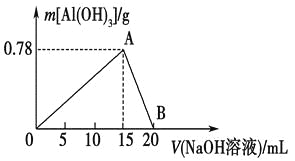
(1)图中A点表示的意义是_________________________。
(2)图中B点表示的意义是_________________________。
(3)上述两步反应用总的离子方程式可表示为:____________________________。
(4)若所得Al(OH)3沉淀0.39 g,则此时用去NaOH溶液的体积为______________。
【答案】生成Al(OH)3沉淀的最大值 Al(OH)3沉淀完全溶解于NaOH溶液中,得到NaAlO2溶液 Al3++4OH-===AlO2-+2H2O 7.5 mL或17.5 mL
【解析】
(1)开始AlCl3与NaOH反应Al3++3OH-=Al(OH)3↓,生成Al(OH)3沉淀,NaOH量逐渐增多,Al(OH)3量逐渐增大,到A点时氢氧化钠将AlCl3恰好完全沉淀时,Al(OH)3沉淀达到最大量;
(2)继续滴加,沉淀逐渐溶解,发生Al(OH)3+OH-=AlO2-+2H2O,B点时沉淀完全溶解于氢氧化钠溶液中,得到NaAlO2溶液;
(3)上述两步反应用总的离子方程式可表示为Al3++4OH-= AlO2-+2H2O;
(4)0.39 g Al(OH)3的物质的量=![]() =0.005mol,当NaOH溶液不足时,生成0.39 g Al(OH)3所需NaOH的物质的量为:0.005mol×3=0.015 mol,需要NaOH溶液的体积=
=0.005mol,当NaOH溶液不足时,生成0.39 g Al(OH)3所需NaOH的物质的量为:0.005mol×3=0.015 mol,需要NaOH溶液的体积=![]() =0.0075L=7.5mL;
=0.0075L=7.5mL;
0.78 g Al(OH)3的物质的量=![]() =0.01mol,Al(OH)3沉淀达到最大量AlCl3与NaOH反应Al3++3OH-=Al(OH)3↓,所需NaOH的物质的量=0.01mol×3=0.03 mol当NaOH溶液过量时,还剩余0.39 g Al(OH)3,剩余0.39 g Al(OH)3溶解可以消耗0.005molNaOH,故共消耗NaOH的物质的量=0.03+0.005mol=0.035 mol,需要NaOH溶液的体积=0.035/2=0.0175L=17.5mL,答案7.5 mL或17.5 mL
=0.01mol,Al(OH)3沉淀达到最大量AlCl3与NaOH反应Al3++3OH-=Al(OH)3↓,所需NaOH的物质的量=0.01mol×3=0.03 mol当NaOH溶液过量时,还剩余0.39 g Al(OH)3,剩余0.39 g Al(OH)3溶解可以消耗0.005molNaOH,故共消耗NaOH的物质的量=0.03+0.005mol=0.035 mol,需要NaOH溶液的体积=0.035/2=0.0175L=17.5mL,答案7.5 mL或17.5 mL


科目:高中化学 来源: 题型:
【题目】实验室欲配制0.5 mol·L-1的NaOH溶液500 mL,有以下仪器:
①烧杯②药匙③1000 mL容量瓶④500 mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)。
(1)配制时,必须使用的仪器有_____(填代号),还缺少的仪器是_____,该实验中两次用到玻璃棒,其作用分别是_____,_____。
(2)使用容量瓶前必须进行的一步操作是_____。
(3)配制时,一般可分为以下几个步骤:①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤⑦定容 ⑧装瓶,其正确的操作顺序是________。
(4)配制一定物质的量浓度的溶液,造成浓度偏高的操作是_____
A.定容时,滴加蒸馏水超过刻度线 B.定容时,眼睛俯视刻度线
C.洗涤烧杯和玻璃棒的溶液未转入容量瓶中 D.定容时,眼睛仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是

A. 两烧杯中H+均移向铜片B. 甲中铜片是负极,乙中锌片发生氧化反应
C. 两烧杯中溶液的pH均增大D. 产生气泡的速度甲比乙慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物YX2、ZX2中,X、Y、Z的核电荷数小于18;X原子最外能层的p能级中有一个轨道充填了2个电子,Y原子的最外层中p能级的电子数等于前一能层电子总数,且X和Y具有相同的电子层数;Z与X在周期表中位于同一主族。回答下列问题:
(1)X的电子排布式为______________,Y的轨道表示式为_________________;
(2)YX2的电子式是______________,分子构型为_________,中心原子发生了____杂化。
(3)Y与Z形成的化合物的分子式是_______,该化合物中化学键是________键(填“极性”或“非极性”),该分子属于__________分子(填“极性”或“非极性”)。
(4)Y的氢化物中分子构型为正四面体的是_______(填名称),键角为_______,中心原子的杂化形式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素的单质X、Y、Z在通常状况下均为气态,并有下列转化关系(反应条件略去):
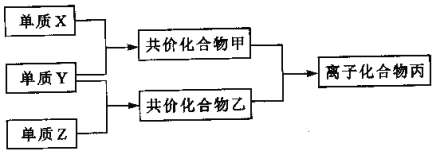
已知:a. 常见双原子单质分子中,X分子含共价健最多。
b. 甲分子含10个电子,乙分子含18个电子,且甲乙相遇可产生大量白烟。
(1)X的结构式是______________,化合物丙的电子式___________________;
(2)实验室可用如图所示装置制备并收集甲。
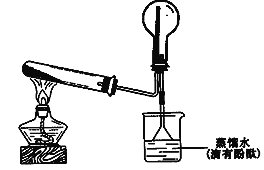
① 写出试管中发生的化学反应方程式__________________;
② 烧杯中溶液由无色变为红色,其原因是(用化学反应方程式来表示)________________。
(3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对图像的叙述正确的是
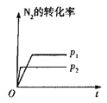
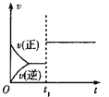
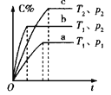
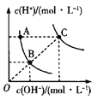
甲 乙 丙 丁
A.图甲可表示压强对反应:![]()
![]() 的影响
的影响
B.图乙中,![]() 时刻改变的条件一定是加入了催化剂
时刻改变的条件一定是加入了催化剂
C.若图丙表示反应:![]() ,则
,则![]() 、
、![]()
D.图丁表示水中![]() 和
和![]() 的关系,ABC所在区域总有
的关系,ABC所在区域总有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据要求填空:
(1)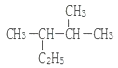 用系统命名法命名:______________;
用系统命名法命名:______________;
(2)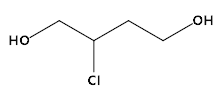 的分子式______________;
的分子式______________;
(3) ![]() 官能团的名称是________________。
官能团的名称是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种食品的配料标签如图所示:
(1)该配料中,富含蛋白质的物质是_________,富含油脂的物质是________;
(2)该配料中的________有防腐作用。碳酸氢钠受热分解,产生的气体使食品膨松,该过程的化学方程式为_________;
(3)用于包装该食品 的聚乙烯塑料包装属于_________(填字母);
a.有机高分子材料 b.无机非金属材料 c.金属材料

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表前四周期的一部分。 X 原子最外层电子数是其内层电子数的3倍。下列说法正确的是

A. TX2、T2 或X3均可用于做杀菌消毒
B. W元素的单质溶于水和汽化都只破坏了分子间作用力
C. 元素T 的非金属性比W强,所以HT的酸性比HW的酸性强
D. YT3在常压、 178℃时升华,所以 YT3 中只含有离子键,而 ZT4中只含有共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com