
 H2(g)+CO2(g) ΔH=-41kJ·mol-1
H2(g)+CO2(g) ΔH=-41kJ·mol-1  CH4(g) ΔH=-73kJ·mol-1
CH4(g) ΔH=-73kJ·mol-1 C(s)+CO2(g) ΔH=-171kJ·mol-1
C(s)+CO2(g) ΔH=-171kJ·mol-1 CH4(g)+H2O(g)。其他条件相同时,H2的平衡转化率在不同压强下随温度的变化如图所示。
CH4(g)+H2O(g)。其他条件相同时,H2的平衡转化率在不同压强下随温度的变化如图所示。
 CH4(g)+H2O(g),平衡时H2的转化率为80%,求此温度下该反应的平衡常数K。(写出计算过程,计算结果保留两位有效数字)
CH4(g)+H2O(g),平衡时H2的转化率为80%,求此温度下该反应的平衡常数K。(写出计算过程,计算结果保留两位有效数字) CH4(g)+2H2O(g) ΔH=-162kJ·mol-1 (3分,热化学方程式2分,数据1分)
CH4(g)+2H2O(g) ΔH=-162kJ·mol-1 (3分,热化学方程式2分,数据1分) CH4(g)+H2O(g)
CH4(g)+H2O(g)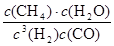 =
=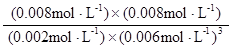 =0.148×106
=0.148×106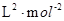
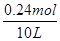 =0.024mol/L,然后结合三段分析如下:
=0.024mol/L,然后结合三段分析如下: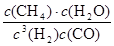 =
=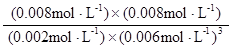 =0.148×106
=0.148×106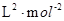 。
。

 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源:不详 题型:单选题
| A.两种元素构成的共价化合物分子中化学键都是极性共价键 |
| B.含有金属元素的化合物一定是离子化合物 |
| C.需要加热才能发生的反应是吸热反应 |
| D.不同元素原子的质量数可能相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X的能量一定低于M的,Y的能量一定低于N的 |
| B.因为该反应为吸热反应,所以需要加热才能使反应进行 |
| C.该反应的能量变化与化学键变化无关 |
| D.X和Y的总能量一定低于M和N的总能量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碳酸钙分解 |
| B.酸碱中和 |
| C.焦碳在高温下与水蒸气反应 |
| D.Ba(OH)2?8H2O与NH4Cl(固体)的反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.△H4=(△H1+△H2-3△H3) | B.△H4=(3△H3-△H1-△H2) |
| C.△H4=(△H1+△H2-3△H3) | D.△H4=(△H1-△H2-3△H3) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1,3-丁二烯和2-丁炔稳定性的相对大小 |
| B.1,3-丁二烯和2-丁炔分子储存能量的相对高低 |
| C.1,3-丁二烯和2-丁炔相互转化的热效应 |
| D.一个碳碳叁键的键能与两个碳碳双键的键能之和的大小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g)ΔH=-1367.0 kJ·mol-1(燃烧热) |
| B.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=+57.3 kJ·mol-1(中和热) |
| C.2NO2===O2+2NO ΔH=+116.2 kJ·mol-1(反应热) |
| D.S(s)+O2(g)===SO2(g) ΔH=-296.8 kJ·mol-1(反应热) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.N2H4(g)+2H2O2(l)=N2(g)+4H2O(l);ΔH=+817.63 kJ·mol-1 |
| B.N2H4(g)+2H2O2(l)=N2(g)+4H2O(g);ΔH=-641.63 kJ·mol-1 |
| C.N2H4(g)+2H2O2(l)=N2(g)+4H2O(l);ΔH=-641.63 kJ·mol-1 |
| D.N2H4(g)+2H2O2(l)=N2(g)+4H2O(g);ΔH=-817.63 kJ·mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com