
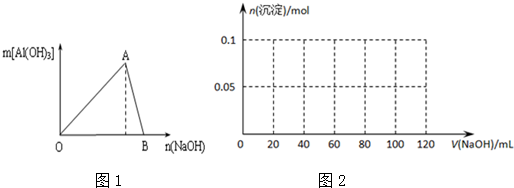
分析 (1)一定量AlCl3溶液中加入NaOH溶液后,随氢氧化钠溶液的加入,先生成氢氧化铝沉淀,达到最大后继续加入氢氧化钠溶液,氢氧化铝沉淀溶解,依据化学方程式的定量关系计算得到;
(2)B处溶液时正好无沉淀,发生反应AlCl3+4NaOH=NaAlO2+2H2O+3NaCl;B处是氢氧化铝溶解生成的偏铝酸钠溶液,通入过量的二氧化碳会反应生成氢氧化铝白色沉淀;
(3)硫酸铝铵是强电解质完全电离;
(4)铵根和铝离子在溶液中共存时,铝离子先和氢氧根离子生成沉淀,然后是铵根离子和碱的反应,接下来是氢氧化铝和氢氧根离子的反应,根据铵根离子、铝离子、偏铝酸根和氢氧根之间的反应的离子方程式确定离子的量的多少;
(5)含有0.1mol NH4Al(SO4)2溶液中含有NH4+离子0.1mol,Al3+物质的量为0.1mol,逐滴加入5mol•L-1 NaOH溶液,发生反应的离子方程式为Al3++3OH-=Al(OH)3↓,NH4++OH-=NH3•H2O,Al(OH)3+OH-=AlO2-+H2O,依据反应的过程和物质的量绘制图象.
解答 解:(1)由图象可知,A点是氯化铝和氢氧化钠反应生成氢氧化铝和氯化钠的反应,反应的化学方程式为:AlCl3+3NaOH=Al(OH)3↓+3NaCl,A点时已参加反应的AlCl3和NaOH的物质的量之比为1:3,
故答案为:3;
(2)B处溶液时正好无沉淀,发生反应AlCl3+4NaOH=NaAlO2+2H2O+3NaCl,故B处溶液中存在的浓度最大的离子为Na+,向B处生成的溶液中通入过量的二氧化碳,可发生反应AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,反应生成白色沉淀,
故答案为:Na+;AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(3)硫酸铝铵是强电解质完全电离,电离方程式为NH4Al(SO4)2=NH4++Al3++2SO42-,
故答案为:NH4Al(SO4)2=NH4++Al3++2SO42-;
(4)加入NaOH溶液,OH-能与NH4+和A13+作用,但由于 A13++3NH3•H2O=A1(OH)3↓+3NH4+,
即碱性NaOH>NH3•H2O>Al(OH)3,则先发生反应的是Al3+与OH-,最后 Al(OH)3逐渐溶解生成A1O2-,
故答案为:①③②⑤④;
(5)含有0.1mol NH4Al(SO4)2溶液中含有NH4+离子0.1mol,Al3+物质的量为0.1mol,逐滴加入5mol•L-1 NaOH溶液,发生反应的离子方程式为:Al3++3OH-=Al(OH)3↓,NH4++OH-=NH3•H2O,Al(OH)3+OH-=AlO2-+H2O,先生成氢氧化铝沉淀需要消耗氢氧化钠物质的量为0.3mol,体积=$\frac{0.3mol}{5mol/L}$=0.060L=60ml,和铵根离子反应消耗氢氧化钠物质的量为0.1mol,氢氧化钠溶液体积=$\frac{0.1mol}{5mol/L}$=0.020L=20ml,生成氢氧化铝沉淀物质的量量为0.1mol,溶解需要氢氧化钠物质的量为0.1mol,消耗氢氧化钠溶液的体积为20ml,依据沉淀量和消耗氢氧化钠溶液体积描出图为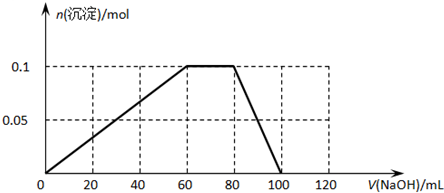 ,
,
故答案为: .
.
点评 本题考查了铝及其化合物性质的分析判断和计算应用,反应的定量关系是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Al3++SO42-+Ba2++3OH-→BaSO4↓+Al(OH)3↓ | |
| B. | Al3++2SO42-+2Ba2++4OH-→BaSO4↓+AlO2- | |
| C. | 2 Al3++3SO42-+3Ba2++6OH-→3BaSO4↓+2Al(OH)3↓ | |
| D. | 4Al3++7SO42-+7Ba2++14OH-→7BaSO4↓+2Al(OH)3↓+2AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol CO2中含有原子数NA | |
| B. | 1 L 1mol/L的硫酸钠溶液中,所含Na+数为NA | |
| C. | 标准状况下,11.2 L水所含分子数为0.5 NA | |
| D. | 1 mol Fe含有原子数NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
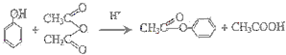
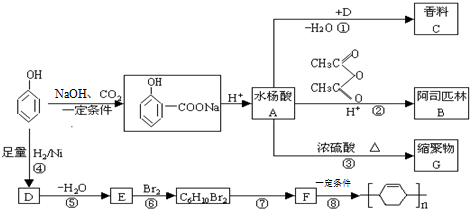
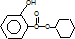 ,G的结构简式
,G的结构简式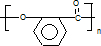 .
.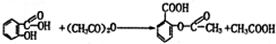 .
.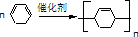 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
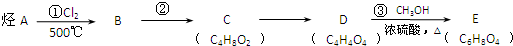
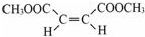 .
.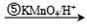 $\stackrel{⑥}{→}$$\stackrel{⑦酸化}{→}$D.则⑥所需的无机试剂及反应条件是NaOH的醇溶液、加热;④的化学方程式是
$\stackrel{⑥}{→}$$\stackrel{⑦酸化}{→}$D.则⑥所需的无机试剂及反应条件是NaOH的醇溶液、加热;④的化学方程式是 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 甲 | 乙 | 丙 |
| ① | CO2 | SO2 | 石灰水 |
| ② | HCl | CO2 | 石灰水 |
| ③ | CO2 | SO2 | Ba(NO3)2 |
| ④ | NO2 | SO2 | BaCl2 |
| ⑤ | CO2 | NH3 | CaCl2 |
| A. | ②③④ | B. | ①③④ | C. | ①②③④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘-131的中子数为78 | B. | 碘-131的质量数为53 | ||
| C. | 碘与铯互称同位素 | D. | 铯-137的质子数为137 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,1LPH=0的硫酸溶液中,H+数为NA | |
| B. | 0.5mol 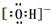 中含有的电子数为4.5NA 中含有的电子数为4.5NA | |
| C. | 7.8gNa2S与Na2O2的混合物中含有的阴离子数目为0.1NA | |
| D. | 0.1mol14N18O与3.1g13C18O的中子数均为1.7NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com